ОРИГИНАЛЬНОЕ ИССЛЕДОВАНИЕ
Применение антимикробной фотодинамической терапии на основе МЦ540 к модели раневой инфекции
1 Отдел медицинской химии и токсикологии, Российский национальный исследовательский медицинский университет имени Н. И. Пирогова, Москва
2 Лаборатория биологических испытаний, Институт трансляционной медицины,Российский национальный исследовательский медицинский университет имени Н. И. Пирогова, Москва
3 Кафедра медицинской кибернетики и информатики, медико-биологический факультет,Российский национальный исследовательский медицинский университет имени Н. И. Пирогова, Москва
4 Лаборатория экологии возбудителей инфекций, Национальный исследовательский центр эпидемиологии и микробиологии имени Н. Ф. Гамалеи, Москва
Фотодинамическая терапия (ФДТ) является альтернативным методом лечения инфекций, позволяющим убивать лекарственно-устойчивые бактерии без повреждения ткани хозяина. В настоящем исследовании использован полирезистентный клинический штамм Pseudomonas aeruginosa PA21 (P. aeruginosa) в модели раневой инфекции на мышах для изучения влияния ФДТ (в водных растворах анионного фотосенсибилизатора Мероцианина 540 (МЦ540): в воде и 0,25 М NaCl) на бактериальную инактивацию и заживление ран. После проведения ФДТ гибель бактерий оценивали путем определения бактериологической нагрузки в ранах, процесс заживления ран контролировали прямым измерением штангенциркулем в двух проекциях, а также проведением патоморфологических исследований послойных срезов инфицированных ран. Полученные результаты показали, что ФДТ в присутствии МЦ540 в растворе хлорида натрия (но не МЦ540 в воде) способна вызывать гибель бактерии, препятствовать их восстановлению и значительно ускорять процесс заживления ран.
Ключевые слова: антимикробная фотодинамическая терапия, полирезистентный клинический штамм Pseudomonas aeruginosa, инфекция кожи и мягких тканей, заживление ран, мероцианин 540, раневая инфекция
Финансирование: исследование выполнено при финансовой поддержке РФФИ в рамках научного проекта № 16-33-00970 мол_а.
Для корреспонденции: Татьяна Анатольевна Шмиголь
ул. Островитянова, д. 1, г. Москва, 117997; moc.liamg@hsithsitat
Кожа служит физическим барьером и первой линией защиты организма от окружающих патогенов. При повреждении кожного покрова в ране может развиться инфекция и остановить процесс заживления раны, приведя к увеличению риска заболеваемости и даже смертности. Открытие антибиотиков произвело революцию в лечении инфекций, но наблюдающееся в последнее время увеличение резистентности к антибиотикам среди патогенных бактерий диктует необходимость поиска новых альтернативных методов лечения локализованных инфекций. Одним из таких методов стала ФДТ, которая ранее успешно применялась в лечении онкологии [1–3], а недавно была предложена для лечения бактериальных инфекций [4–7]. Суть антимикробной ФДТ заключается в местном применении в инфицированной ткани нетоксичного красителя — фотосенсибилизатора (ФС) с последующим воздействием монохроматическим светом с длинной волны, к которой чувствителен ФС [8–9]. Под действием света ФС активируется, генерируя свободные радикалы и/или синглетный кислород, губительные для инфекционных агентов.
Цель настоящего исследования заключалась в изучении влияния ФДТ с использованием анионного ФС МЦ540 в модели раневой инфекции на животных на бактериальную инактивацию и на процесс заживления ран. Мыши линии BALB/c были инфицированы полирезистентным клиническим штаммом Pseudomonas aeruginosa PA21. Инактивацию бактерий оценивали путем определения бактериологической нагрузки в ранах, процесс заживление ран контролировали прямым измерением штангенциркулем в двух проекциях, а также проведением патоморфологических исследований послойных срезов инфицированных ран.
МАТЕРИАЛЫ И МЕТОДЫ
Фотосенсибилизатор
Маточный раствор МЦ540 (Sigma-Aldrich, Швейцария) в концентрации 1×10–3 M готовили в 96% этаноле в день проведения опыта. Концентрацию МЦ540 определяли спектрофотометрически с использованием коэффициента экстинкции ε500 = 63 000 М–1см–1 в воде. В рабочих растворах концентрация МЦ540 составляла 25 мкМ, которую получали путем разведения маточного раствора МЦ540 (1×10–3 M) водой или 0,25 М раствором NaCl (ACROS, США).
Культуры клеток микроорганизмов
В работе использовали полирезистентный клинический штамм Pseudomonas aeruginosa PA21 из коллекции микроорганизмов ФГБУ ФНИЦ эпидемиологии и микробиологии имени Н. Ф. Гамалеи. P. aeruginosa инкубировали в течение ночи при 37 °C в питательном бульоне Brain Heart Infusion (BHI «Difco», США), разводили в свежей питательной среде 1:100, растили до оптической плотности (OD600), равной 1, что соответствует концентрации 109 КОЕ/мл. Далее культуру дважды отмывали фосфатно-солевым буфером (pH = 7,4) (Экосервис, Россия) и аликвотами по 50 мкл наносили на рану.
Бактериальная нагрузка ран
Отбор материала производили по следующей методике: при помощи ватных тампонов получали мазок непосредственно с поверхности раны. Далее тампон помещали в пробирку с 0,9 мл физиологического раствора, из которого в последующем готовили серийные разведения 1:10, 1:100, 1:1000. Каждое разведение высевали на две чашки с агаризованной средой (BHI «Difco», США), подсчет колоний проводили через 24 ч, результаты выражали в колониеобразующих единицах (КОЕ), а именно в десятичном логарифме, взятом от количества КОЕ.
Антимикробная фотодинамическая терапия
Манипуляции во время проведения экспериментов выполняли с соблюдением правил асептики и антисептики с использованием щадящей методики обезболивания. Все исследования проводили с соблюдением правил биоэтики и международных принципов и требований «Европейской конвенции по защите позвоночных животных» (Страсбург, март 1986 г.) и Хельсинской декларации о гуманном отношении к животным. В исследовании использовали мышей BALB/c 6–8 недель и весом 17–21 г. За сутки до проведения ФДТ на спине животных выбривали участок кожи площадью 2 см2 и затем перманентным маркером намечали контур будущей раны. Перед формированием раны животным давали ингаляционный наркоз (изофлуран). Поверхность кожи дважды обрабатывали антисептиком, наносили рану округлой формы 1,5 см в диаметре, иссекали кожу, подкожную клетчатку и фасцию до мышц. Далее на рану наносили аликвоту объемом 50 мкл, содержащую суспензию бактерий (P. aeruginosa) в концентрации 107 КОЕ/мл. Через 6 ч после инокуляции бактерий проводили ФДТ.
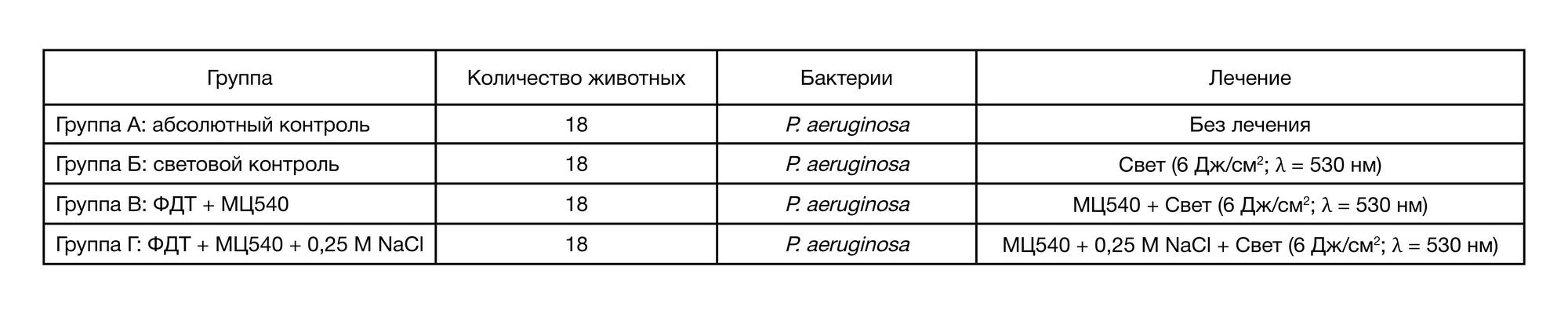
Животных разделили на 4 группы (табл. 1). Мыши из группы А (n = 18) служили в качестве абсолютного контроля, не получая никакого лечения; мыши из группы Б (n = 18) служили в качестве светового контроля и для лечения инфицированной раны облучались монохроматическим светом с длиной волны 530 нм и временем экспозиции 5 мин; мыши группы В (n = 18) получали ФДТ в присутствии 25 мкМ водного раствора МЦ540 с облучением монохроматическим светом с длиной волны 530 нм и временем экспозиции 5 мин; мыши группы Г (n = 18) получали ФДТ в 25 мкМ водном растворе МЦ540 в присутствии 0,25 М NaCl с облучением монохроматическим светом с длиной волны 530 нм и временем экспозиции 5 мин. Из каждой группы было оставлено по 3 животных для наблюдения за долгосрочными эффектами (36 сут.).
Мышей обрабатывали локально 50 мкл раствора 25 мкМ в 0,25 M NaCl, с экспозицией без облучения в течение 5 мин. Обработанные очаги были освещены светом с длиной волны 530 нм, обеспечивающим 2 мВт/см2 в течение 5 мин, что соответствует общей дозе 6 Дж/см2.
Гистология
Биологический материал фиксировали в буферном растворе 10%-го формалина. Фиксированные образцы заключали в парафин. Срезы толщиной 3–7 мкм окрашивали гематоксилин-эозином и использовали для микроструктурного анализа и морфометрических наблюдаемых процессов. Морфометрические данные были получены с помощью микроскопа-анализатора AxioimagerA-2 (Carl Zeiss, Германия).
Заживление раневого дефекта
При наблюдении за состоянием раневых дефектов оценивали наличие признаков воспаления, характер и количество раневого отделяемого и т. д. Измерение ран с помощью линейки и штангенциркуля в двух проекциях осуществляли за 1 ч до проведения ФДТ на 2-е, 4-е, 7-е и 14-е сут. Для выявления характера течения репаративных процессов в исследуемых группах животных вычисляли следующие показатели динамики заживления экспериментальных ран:
- Показатель изменения площади раневой поверхности в динамике (ΔS, %) : форм. 1 где S0 — исходная площадь раны, Sn — площадь раны на n-е сутки.
- Относительная скорость уменьшения площади раневого дефекта (νзаж., %/сутки): форм. 2 где S0 — исходная площадь раны, Sn — площадь раны на n-е сутки, n — порядковый номер суток эксперимента.
- Показатель скорости эпителизации раны (νэпит., мм2 / сутки): форм. 3, где S0 — исходная площадь раны, Sn — площадь раны на n-е сутки, Т — число суток между измерениями.
Все цифровые данные обрабатывали с использованием компьютерной программы Universlab DeskTer River V3.3.3269.
Статистика
Рассчитывали средние значения определяемых величин и стандартную ошибку среднего по форм. 4 где s — выборочное среднее квадратичное отклонение.
РЕЗУЛЬТАТЫ
На следующие сутки после моделирования ран и проведения ФДТ общее состояние животных можно было оценить как удовлетворительное. Животные были активны, слизистые оболочки без видимых изменений, шерстный покров гладкий. Раны у всех животных имели признаки развивающегося нагноения. Наиболее выраженное нагноение наблюдалось в контрольных группах.
Бактериальная нагрузка
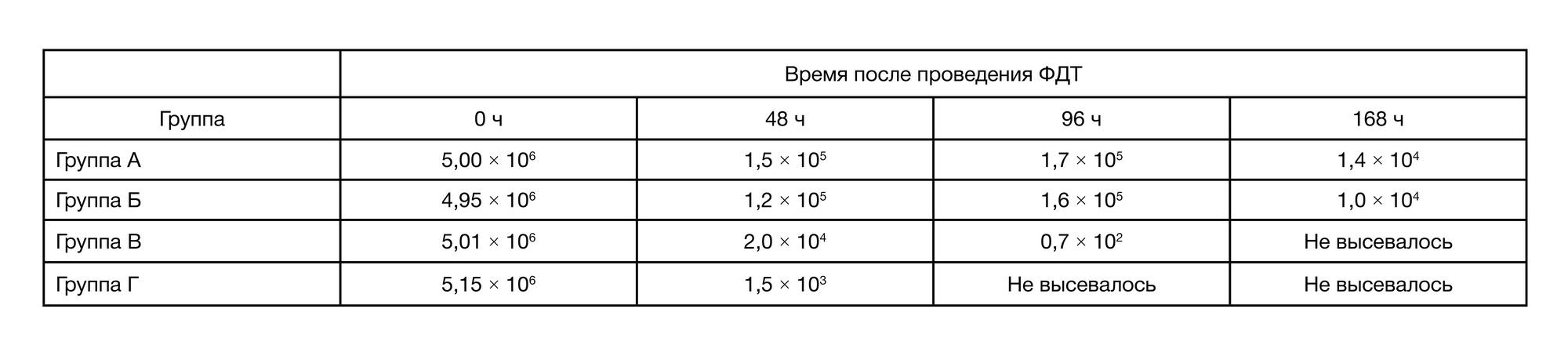
Одним из значимых критериев оценки эффективности проведенного лечения гнойных ран мягких тканей является микробиологическое исследование. Определение бактериальной нагрузки производилось до начала проведения лечения, через 48, 96 и 168 ч после ФДТ. Количественные показатели бактериальной нагрузки ран представлены в табл. 2.
Через 6 ч после инфицирования перед ФДТ исходная контаминация ран во всех группах животных была одинаковой и составила 5,03 ± 0,04×106 КОЕ/мл. В опытных группах В (ФДТ индуцированная МЦ540 в воде) и Г (ФДТ индуцированная МЦ540 в растворе натрия хлорида) через 48 ч после проведения ФДТ количество P. aeruginosa уменьшилось на 102 и 103 КОЕ/мл соответственно.
Сравнительная характеристика течения инфицированных раневых дефектов
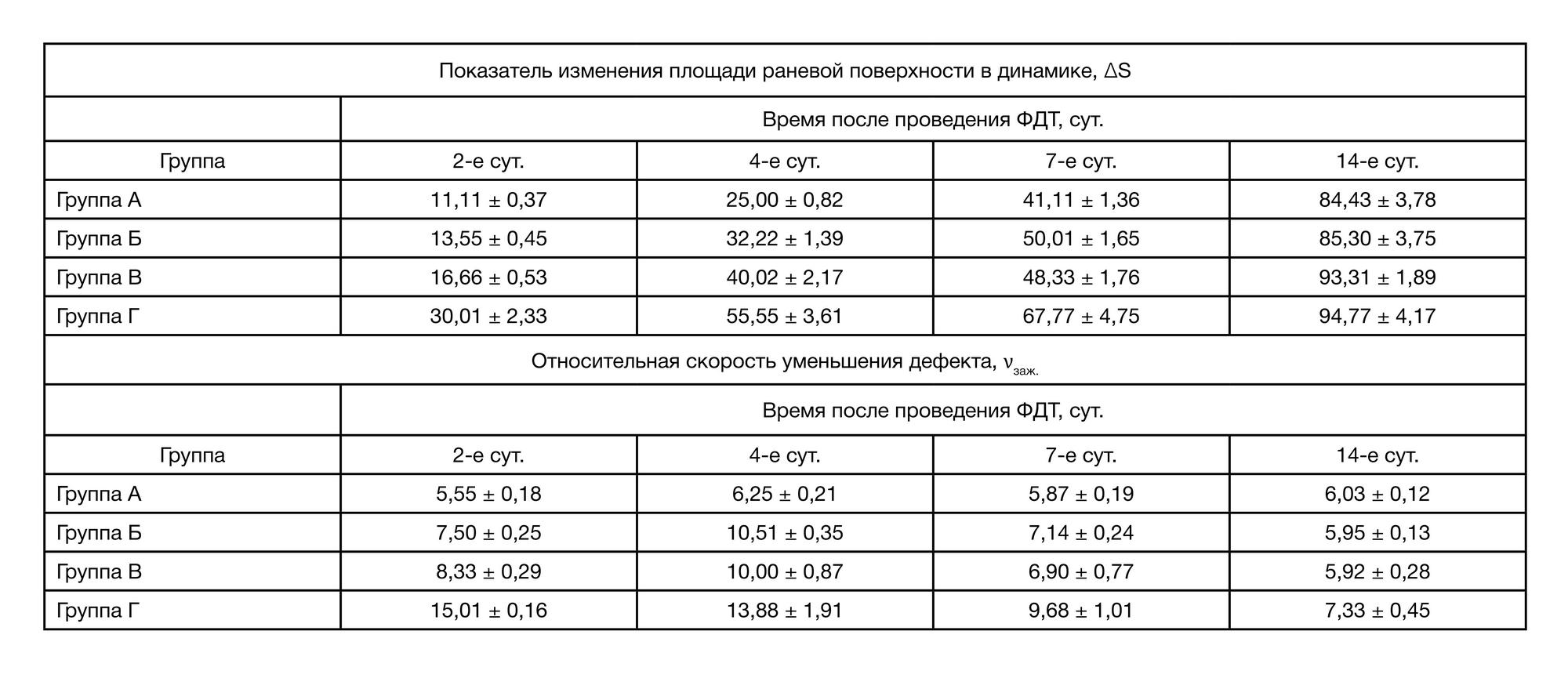
Сравнительный анализ результатов наблюдения характеристик течения раневых дефектов в экспериментальных группах позволил установить межгрупповые различия динамики заживления раневых дефектов по показателю ΔS (табл. 3).
Анализ полученных данных показал, что значения ΔS контрольных групп А и Б достоверно меньше (p < 0,05) соответствующих показателей опытных групп В и Г на всех этапах проведения эксперимента (исключение составило отсутствие значимых различий с результатом группы Б и В на 7-е сут.).
Сравнительный анализ скоростей заживления раневых дефектов в динамике выявил значимые внутригрупповые различия показателей νзаж. (см. табл. 3). Из полученных данных видно, что наибольшая скорость заживления наблюдается в группе Г, а в остальных группах на протяжении 14 сут., показатели νзаж. находились на достаточно стабильном уровне (p > 0,05). Отметим, что скорость заживления к 14 сут. снижается и становится практически одинаковой для всех групп.
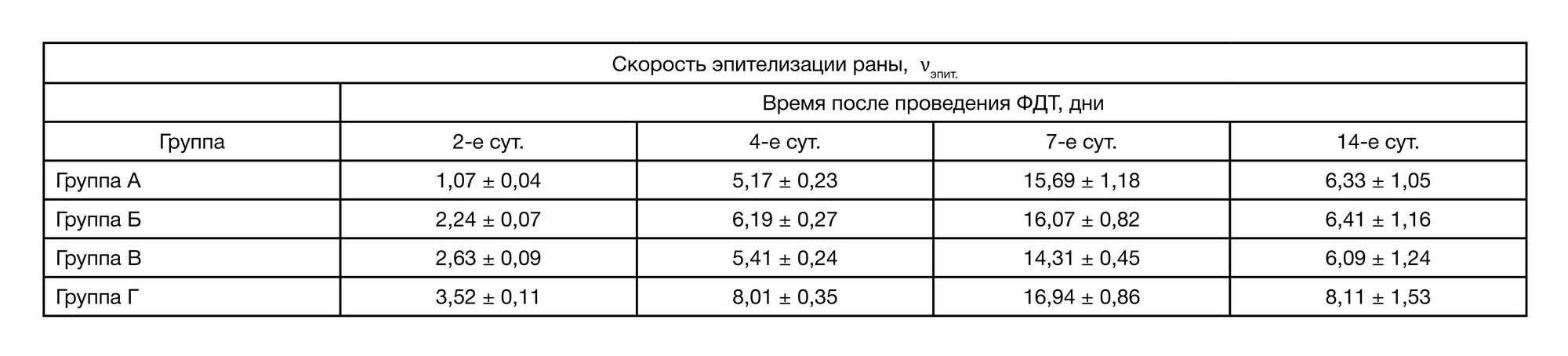
Нами выявлены существенные изменения, а также межгрупповые различия показателей скорости эпителизации раневых дефектов (νэпит.) в процессе проведения эксперимента (табл. 4).
Максимальные значения скорости эпителизации (νэпит.) в интервале 4–7 сутки были отмечены в группе Г (p < 0,05 во всех случаях), к 14 сут. скорость эпителизации во всех группах снижалась.
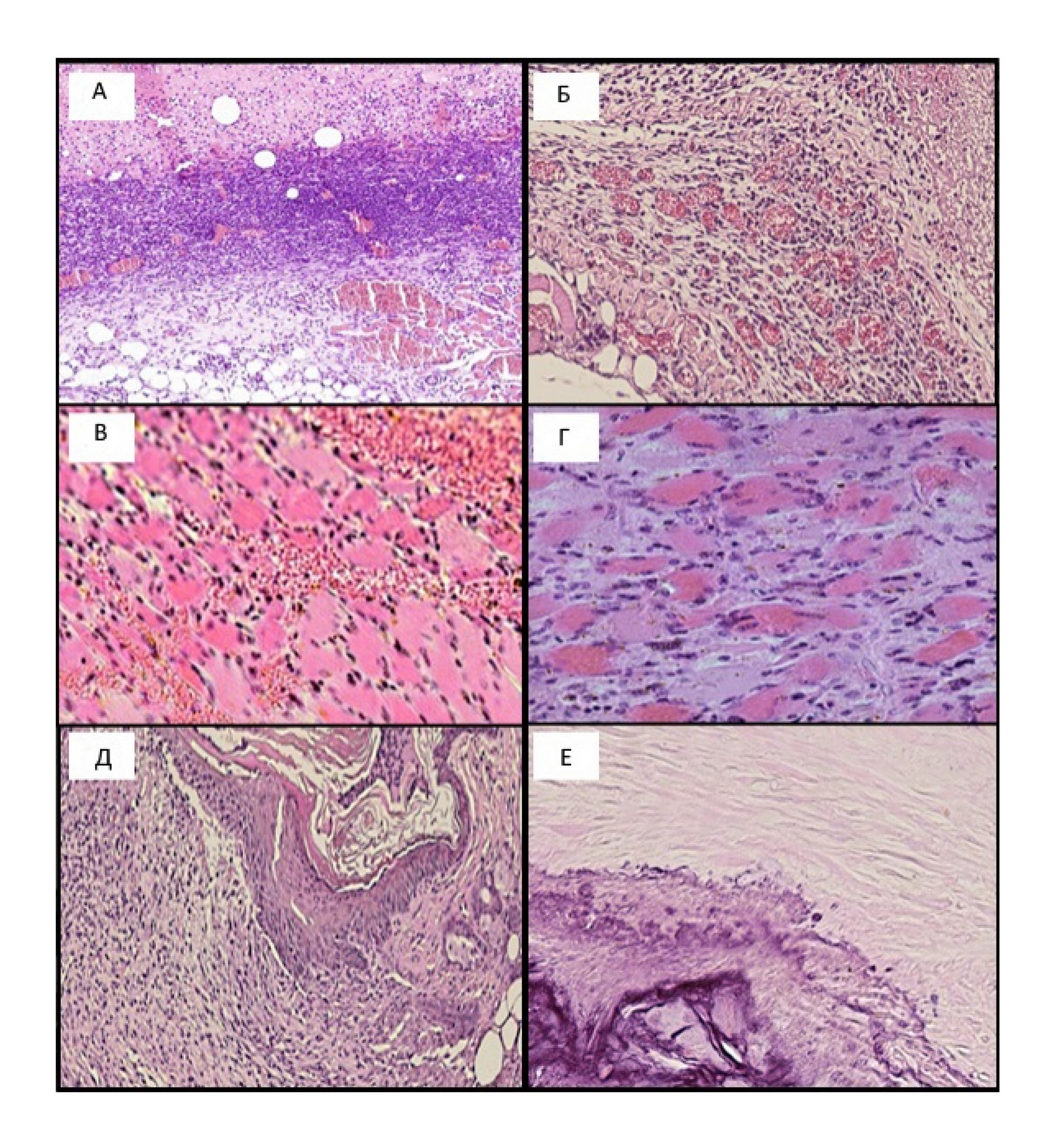
В первые 48 ч в ране происходят изменения, характеризующиеся формированием кровяного сгустка. В основе сгустка лежит фибрин, который формирует струп с выпотом экссудата и клеточных элементов с преобладанием нейтрофилов. Наступает лизис форменных элементов крови с формированием всех признаков гнойного воспаления (рисунок 1А).
Под лизирующимся струпом бурно разрастается молодая соединительная ткань в основе которой выявляются многочисленные тонкостенные капилляры, синусы, лакуны, заполненные большим количеством крови (рисунок 1Б). Со временем (4–7 сут.) вновь образованная соединительная ткань превращается в рубцовую, порой гиализированную и даже петрифицированную (рисунок 1Е). Даже неглубоко расположенные такие инфильтраты вызывают контрактуры, и, следовательно, приводят к неподвижности кожи.
В это же время в гистологических препаратах выявлялось медленное (24–48 ч), а затем бурное размножение базальных клеток эпидермиса с нарастающей его кератинизацией. Разрастаясь и дифференцируясь, эпидермис постепенно закрывает дефект кожи (табл. 4, рисунок 1Д). Синтетические процессы в ране проходят равнонаправленно, но с определенным сдвигом во времени. На эти процессы влияет много факторов, в том числе заданные экспериментом (табл. 3 и табл. 4, рисунок 1). Обилие крови, усиленная оксигенация и обилие ферментативных процессов в ране, возникающие со временем, усиливают процесс неполной репаративной регенерации. Протекающий процесс вызывает даже внутриклеточную регенерацию миосателлитов (табл. 3 и табл. 4, рисунок 1Г).
Таким образом, микроструктурный анализ хорошо коррелирует с полученными данными (табл. 2 – табл. 4, рисунок 1) и указывает на бурное заживление ран за счет активного роста, дифференцировки и созревания микрососудистого русла с формированием грануляционной ткани, а также усиленной эпителизации раневого дефекта.
ОБСУЖДЕНИЕ
В исследованиях in vitro ранее нами было показано, что в случае ФДТ МЦ540 в присутствии 0,25 М NaCl инактивация P. aeruginosa возрастает в 10 раз по сравнению с ФДТ МЦ540 в воде [10]. Наблюдаемый эффект был объяснен разной степенью агрегации МЦ540 в воде и в присутствии соли. В воде МЦ540 находится как в мономерной, так и димерной формах [11], из которых только мономерная форма способна генерировать активные формы кислорода, в первую очередь — синглетный кислород [12, 13]. В солевых растворах МЦ540 образует крупные кристаллоподобные агрегаты, способные к генерации свободных радикалов [14–17].
Представленные в настоящем исследовании данные на животных моделях убедительно подтвердили ранее полученные данные in vitro по следующим показателям: гибель бактерий, препятствование их восстановлению и ускорение процесса заживления ран.
Действительно, согласно представленным в табл. 2 данным, после проведенной ФДТ с МЦ540 в растворе натрия хлорида полное очищение раны от полирезистентного штамма P. aeruginosa происходит к 4 сут., тогда как при проведении ФДТ с МЦ540 в воде аналогичные изменения наблюдались лишь на 7-е сут.
Морфометрические данные (табл. 3) подтверждают лучшую эффективность агрегатов МЦ540 по сравнению с его мономерами и димерами в отношении скорости заживления раневого дефекта и уменьшения его площади. Так, к 4 сут. площадь раневого дефекта у животных из группы Г уменьшилась на 45%, в то время как для группы В эта величина составляет 60%, что близко к показателям группы Б (68%).
Наблюдаемые изменения относительной скорости уменьшения дефекта (табл. 3) в случае группы А имеют практически линейную зависимость (с учетом среднеквадратичного отклонения), для групп Б–В — параболическую с максимумом на 4-е сут., а для группы Г — экспоненциальную. Для животных всех исследованных групп на 14-е сутки наблюдалось снижение скорости заживления. Полученные данные согласуются с описанным ранее изменением показателя площади раневой поверхности (табл. 3).
Регенерация эпителиального покрова ран происходит значительно быстрее, и становиться ярко выраженной уже на 4-е сут. в группе Г (см. табл. 4), в отличии не только от контроля, но и группы, получившей лечение на основе ФДТ с МЦ540 в воде.
Микроструктурный анализ хорошо коррелирует с полученными данными (табл. 2– табл. 4, рисунок) и указывает на бурное заживление ран за счет активного роста, дифференцировки и созревания микрососудистого русла с формированием грануляционной ткани, а также усиленной эпителизации раневого дефекта. Однако, хотя процессы заживления, а также очищения раны от патогенных бактерий происходили намного быстрее в случае применения ФДТ с МЦ540 в растворе хлорида натрия, сам процесс происходит «жестче» с расплавлением фибрина и образованием фибриноида. Для ФДТ с МЦ540 в воде процесс заживления проходит медленнее, «мягче» и без активного образования фибриноида.
ВЫВОДЫ
Согласно данным, полученным в модели раневой инфекции на мышах, ФДТ с МЦ540 в растворе хлорида натрия способна намного эффективнее вызывать гибель бактерий, препятствовать их последующему восстановлению и значительно ускорять процесс заживления ран, по сравнению с контрольными группами и ФДТ с МЦ540 в воде.
- Fakayode OJ, Tsolekile N, Songca SP, Oluwafemi OS. Applications of functionalized nanomaterials in photodynamic therapy. Biophys. 2018; 2. doi: 10.1007/s12551-017-0383-2.
- Rundle P. Photodynamic Therapy for Eye Cancer. Biomedicines. 2017; 5 (4): 69.
- Meimandi M, Talebi Ardakani MR, Esmaeil Nejad A, Yousefnejad P, Saebi K, Tayeed MH. The Effect of Photodynamic Therapy in the Treatment of Chronic Periodontitis: A Review of Literature. J Lasers Med Sci. 2017; 8 (1): 7–11.
- Demidova TN, Hamblin MR. Photodynamic therapy targeted to pathogens. Int J Immunopathol Pharmacol. 2004; 17: 245–54.
- Hamblin MR, Hasan T. Photodynamic therapy: a new antimicrobial approach to infectious disease? Photochem Photobiol Sci. 2004; 3: 436–50.
- Hamblin MR. Antimicrobial photodynamic inactivation: a bright new technique to kill resistant microbes. Curr Opin Microbiol. 2016; 33: 67–73.
- Neundorf I. Reinhardt A. Design and Application of Antimicrobial Peptide Conjugates. Int J Mol Sci. 2016; 17 (5): 701.
- Joseph B, Janam P, Narayanan S, Anil S. Is Antimicrobial Photodynamic Therapy Effective as an Adjunct to Scaling and Root Planing in Patients with Chronic Periodontitis? A Systematic Review Biomolecules. 2017; 7 (4): 79.
- Liu CC, Zhao JJ, Zhang R1, Li H, Chen B, Zhang LL et al. Multifunctionalization of graphene and graphene oxide for controlled release and targeted delivery of anticancer drugs. Am J Transl Res. 2017; 9 (12): 5197–219.
- Шмиголь Т. А., Бехало В. А., Сысолятина Е. В., Нагурская Е. В., Ермолаева С. А., Потапенко А. Я. Влияние хлорида натрия на агрегацию мероцианина 540 и фотосенсибилизированную инактивацию Pseudomonas aeruginosa и Staphylococcus aureus. Acta Naturae. 2011: 112–118.
- Bilski P, McDevitt T, Chignell CF. Merocyanine 540 solubilized as an ion pair with cationic surfactant in nonpolar solvents: spectral and photochemical properties. Photochem Photobiol. 1999; 69 (6): 671–676.
- Levard C, Hotze EM, Lowry GV, Brown GE Jr. Environmental transformations of silver nanoparticles: impact on stability and toxicity. Environ Sci Technol. 2012; 3; 46 (13): 6900–14.
- Kepczynski M, Dzieciuch M, Nowakowska M. Nano-structural hybrid sensitizers for photodynamic therapy. Curr Pharm Des. 2012; 18 (18): 2607–21.
- Ragàs X, Xin He, Agut M, Roxo-Rosa M, Rocha Gonsalves A, Arménio C. Serra et al. Singlet Oxygen in Antimicrobial Photodynamic Therapy: Photosensitizer-Dependent Production and Decay in E. coli. Molecules. 2013; 18 (3): 2712–25.
- Yin R, Dai T, Avci P, Jorge AE, de Melo WC, Vecchio DH. et al. Light based anti-infectives: ultraviolet C irradiation, photodynamic therapy, blue light, and beyond. Curr Opin Pharmacol. 2013; 13: 731–62.
- Vatansever F, de Melo WC, Avci P, et al. 2013. Antimicrobial strategies centered around reactive oxygen species — Bactericidal antibiotics, photodynamic therapy, and beyond. FEMS Microbiol Rev. 2013; 37 (6): 955–89.
- Avci P, Erdem SS, Hamblin MR. Photodynamic Therapy: One Step Ahead with Self-Assembled Nanoparticles J Biomed Nanotechnol. 2014; 10 (9): 1937–52.