ОРИГИНАЛЬНОЕ ИССЛЕДОВАНИЕ
Электромиостимуляция как альтернатива физической тренировке у пациентов с ХОБЛ
1 Кафедра госпитальной терапии, педиатрический факультет, Российский национальный исследовательский медицинский университет имени Н. И. Пирогова, Москва
2 Кафедра пульмонологии, факультет дополнительного профессионального образования, Российский национальный исследовательский медицинский университет имени Н. И. Пирогова, Москва
3 Городская клиническая больница имени Д. Д. Плетнева, Москва
Пациенты с обострением хронической обструктивной болезни легких (ХОБЛ) не способны выполнять тренировочные упражнения в рамках программы легочной реабилитации. Альтернативой служит метод электромиостимуляции (ЭМС), поскольку его применение не вызывает усиления одышки у пациента. Целью работы была оценка эффективности краткосрочной ЭМС четырехглавой мышцы бедра на двигательную активность у пациентов с ХОБЛ. В проспективное открытое рандомизированное исследование вошли 36 пациентов, разделенные на две сопоставимые группы. Пациентам в основной группе проводили ЭМС в течение 10 дней. На 10-е сутки регистрировали и сравнивали клинико-функциональные параметры и потенциальные побочные эффекты. Между двумя группами не было отмечено существенных различий в отношении исходных характеристик. По результатам межгруппового анализа, основная группа имела статистически значимые улучшения показателей измерений, выполненных шагомерм и при миографии, равных соответственно 418,5 (86,0; 815,0) против 226,7 (48,0; 660,0) (p = 0,02), 463,0 (122; 804) против 210,5 (64; 481) (p = 0,0001). Отмечалось значительное снижение баллов при оценке ХОБЛ по CAT-тесту и оценке одышки по mMRC-шкале и по шкале Borg: 22,8 (18,0; 34,0) против 28,4 (26,0; 34,0) (p = 0,00007), 2,7 (2,0; 4,0) против 3,1 (3,0; 4,0) (p = 0,03) и 6,3 (5,0; 7,0) против 7,2 (6,0; 9,0) (p = 0,0002) соответственно. Побочных эффектов в основной группе отмечено не было. На основании полученных результатов можно сделать вывод, что краткосрочная ЭМС четырехглавой мышцы бедра улучшает двигательную активность пациентов, повышая качество жизни и способность выполнять программы легочной реабилитации в последующем, и является альтернативой физическим тренировкам у пациентов с ХОБЛ.
Ключевые слова: легочная реабилитация, обострение ХОБЛ, дисфункция скелетной мускулатуры, электромиостимуляция
Для корреспонденции: Татьяна Викторовна Кунафина
ул. Островитянова, д. 1, г. Москва, 117997; ur.liam@70_anat
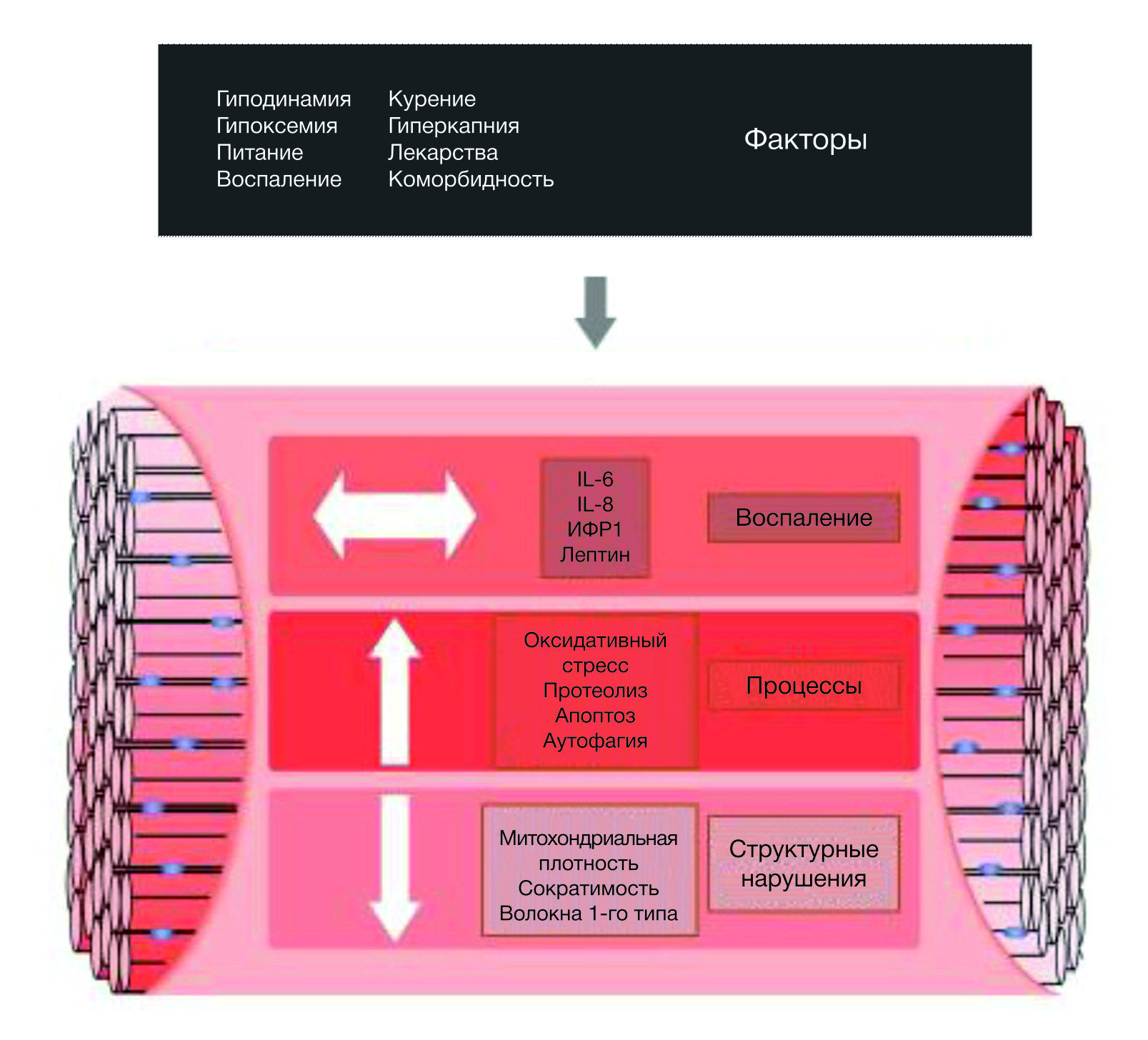
Хроническая обструктивная болезнь легких (ХОБЛ) является одной из ведущих причин заболеваемости и смертности во всем мире [1, 2]. Естественное течение заболевания отмечено обострениями, которые влияют на прогноз у таких пациентов [2]. Становится все более очевидным, что ХОБЛ присущ ряд системных проявлений, особенно при тяжелом протекании заболевания, и что эти проявления оказывают выраженное влияние на выживаемость пациентов и развитие сопутствующих заболеваний. У пациентов с тяжелой формой ХОБЛ часто отмечается кахексия. Возможна потеря мышечной массы и слабость мышц в результате активации апоптоза и/или бездействия мышц [3, 4]. При обострении заболевания отмечается увеличение дыхательной недостаточности, а также возрастает потребность в системных глюкокортикостероидах, при этом усугубляется и без того плохое состояние скелетной мускулатуры. Это, в свою очередь, приводит к утомлению дыхательной мускулатуры с одной стороны, и к ограничению двигательной активности — с другой. При уменьшении двигательной активности отмечается гиподинамия, приводящая к дистрофии, а в последующем — к атрофии скелетных мышц (рис. 1). Одной из самых крупных мышц, участвующих в двигательной активности является четырехглавая мышца бедра. Слабость и атрофия именно этой мышцы приводят к худшим прогнозам и повышению смертности у пациентов с ХОБЛ [4].
Из-за развивающейся слабости и атрофии скелетной и дыхательной мускулатуры у больных с тяжелой формой ХОБЛ, в терапии таких пациентов отводится большое значение физической тренировке [5, 6]. Физические тренировки — основной компонент легочной реабилитации. Продолжительность тренировок может достигать 4–12 недель, оптимальным сроком считают 6–8 недель [6]. Легочная реабилитация на протяжении не менее 4 недель приводит к улучшению клинически и статистически значимых показателей качества жизни, в том числе уменьшению одышки, усталости, улучшению эмоционального статуса [7]. Однако пациенты с тяжелой и крайне тяжелой степенью ХОБЛ не способны к выполнению данных методов реабилитации из-за выраженной дыхательной недостаточности, общей слабости, низкой готовности к легочной реабилитации. В качестве альтернативы и «мостиком» к физическим тренировкам является электромиостимуляция [7]. Показана эффективность электромиостимуляции четырехглавой мышцы бедра, проводившейся на протяжении не менее 4 недель, в качестве оценки которой использовали шкалы по определению одышки и опросник Святого Георгия (St. George's Respiratory Questionnaire) [8].
Целью нашего исследования была оценка эффективности краткосрочного воздействия электромиостимуляции на четырехглавую мышцу бедра с применением шагомера и метода поверхностной электромиографии у пациентов с тяжелым течением и обострением ХОБЛ, не способных к выполнению стандартных программ легочной реабилитации.
ПАЦИЕНТЫ И МЕТОДЫ
В период с сентября 2016 г. по февраль 2018 г. в пульмонологическом отделении университетской клиники проводили открытое проспективное когортное рандомизированное сравнительное исследование. Обследовали 56 пациентов с обострением ХОБЛ, сопровождающимся духательной недостаточностью. Из них только у 36 пациентов была зафиксирована дисфункция четырехглавой мышцы бедра. Пациенты были разделены на две группы. В основной группе (n = 18) проводили краткосрочную электромиостимуляцию с помощью аппарата Compex (Compex, Франция). Результаты сопоставляли попарно с контрольной группой (n = 18). Критериями включения пациентов были обострение ХОБЛ, определяемое клинически по наличию не менее двух признаков и симптомов: нарастанию одышки, усилению кашля, увеличению количества или гнойности мокроты; признаки дыхательной недостаточности, сопровождающиеся слабостью, ограничением физической активности, подтвержденным результатами использования шагомера и метода электромиографии; дисфункция четырехглавой мышцы бедра (амплитуда при максимальном мышечном сокращении по данным поверхностной миографии <600 мкВ). Критерии исключения из исследования: гипертермия до фебрильных и субфебрильных значений температуры; отсутствие изменений на электромиографии; наличие пневмонии; психические нарушения, препятствующие установлению продуктивного контакта между врачом и пациентом; абсолютные противопоказания к применению аппарата, т. е. наличие кардиостимулятора, эпилепсия, серьезные нарушения артериального кровоснабжения нижних конечностей, наличие у пациента брюшной или паховой грыжи. Проведение исследования было одобрено локальным этическим комитетом (протокол №154 от 11.04.2016 г.). От всех пациентов было получено письменное информированное согласие на участие в исследовании.
Пациентов сопоставляли по возрасту, данным опросника mMRC (опросник Британского медицинского исследовательского совета для оценки тяжести одышки), CAT-тесту оценки ХОБЛ, спирометрическим параметрам (объему форсированного выдоха за 1 с (ОФВ1), соотношению ОФВ1/ФЖЕЛ), параметрам газового анализа артериальной крови (ГАК), а именно pH, парциальному давлению кислорода в артериальной крови (PaO2), парциальному давлению углекислого газа в артериальной крови (PaCO2), показателям электромиографии на момент поступления. Все пациенты получали стандартное лечение, назначаемое при обострении ХОБЛ в соответствии с международными рекомендациями (GOLD, 2017): ингаляционные бронхолитики, системные глюкокортикостероиды (преднизолон 20–40 мг в день) и эмпирическую антибактериальную терапию в соответствии с местной бактериальной устойчивостью и сопутствующими заболеваниями. Клинические параметры, показатели шагомера, электромиографии, шкалы одышки по Borg, mMRC, CAT, потенциальные побочные эффекты оценивали по истечении 10 дней и затем сравнивали между двумя группами.
Электромиография
Всем больным из основной группы и группы контроля проводили поверхностную электромиографию (ЭМГ) — метод клинической электромиографии для исследования накожной суммарной биоэлектрической активности мышц в покое и при различных режимах напряжения согласно инструкции производителя. Электромиографию проводили с помощью многофункционального аппарата Nemus 1 (EB Neuro; Италия) с возможностью проведения ЭМГ и вызванных потенциалов.
Забор крови для ГАК
Забор крови производили с помощью автоматически наполняющихся шприцев (PICO70® Radiometer; Дания) из лучевой артерии не ранее чем через 15 мин после прекращения оксигенотерапии и анализировали с помощью анализатора крови RAPIDLab® 1200 Systems (Siemens; Германия) согласно инструкции производителя.
Шагомер
Физическую активность оценивали с помощью шагомера Torneo A-946BTRN (Compus pro; Китай). Аппарат для оценки количества шагов располагался на поясе одежды в течение 6 ч бодрствования.
Электромиостимуляция
Пациентам основной группы проводили электромиостимуляцию. Во время проведения процедуры пациент находился в положении сидя, либо в положении лежа на спине с валиком под коленями (пациенты с крайне тяжелой формой ХОБЛ). (+)-Электрод накладывали на кожу бедра на уровне моторной точки мышцы, где происходило наилучшее сокращение мышцы в условиях максимального комфорта. (–)-Электрод накладывали дистальнее на 10 см. Использовали чередование программ Sport| resistance (спорт, сопротивление), время работы аппарата 32 мин, и Aesthetic, firing (эстетика, укрепление), время работы аппарата 22 мин, через день. Интенсивность подбирали индивидуально по переносимости и ответному мышечному сокращению, в диапазоне от 10 до 35 мА.
Статистический анализ
Статистический анализ проводили с помощью программы Staistica 10 StatSoft. Использовали непараметрические методы описательной статистики: рассчитывали медианы (Ме), верхний (Q3) и нижний (Q1) квартили. Данные представляли в виде (Me (Q1; Q3)). Сравнение двух независимых групп количественных признаков проводили с применением U-теста Манна–Уитни. Статистически достоверными считали различия при р < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Основные характеристики больных
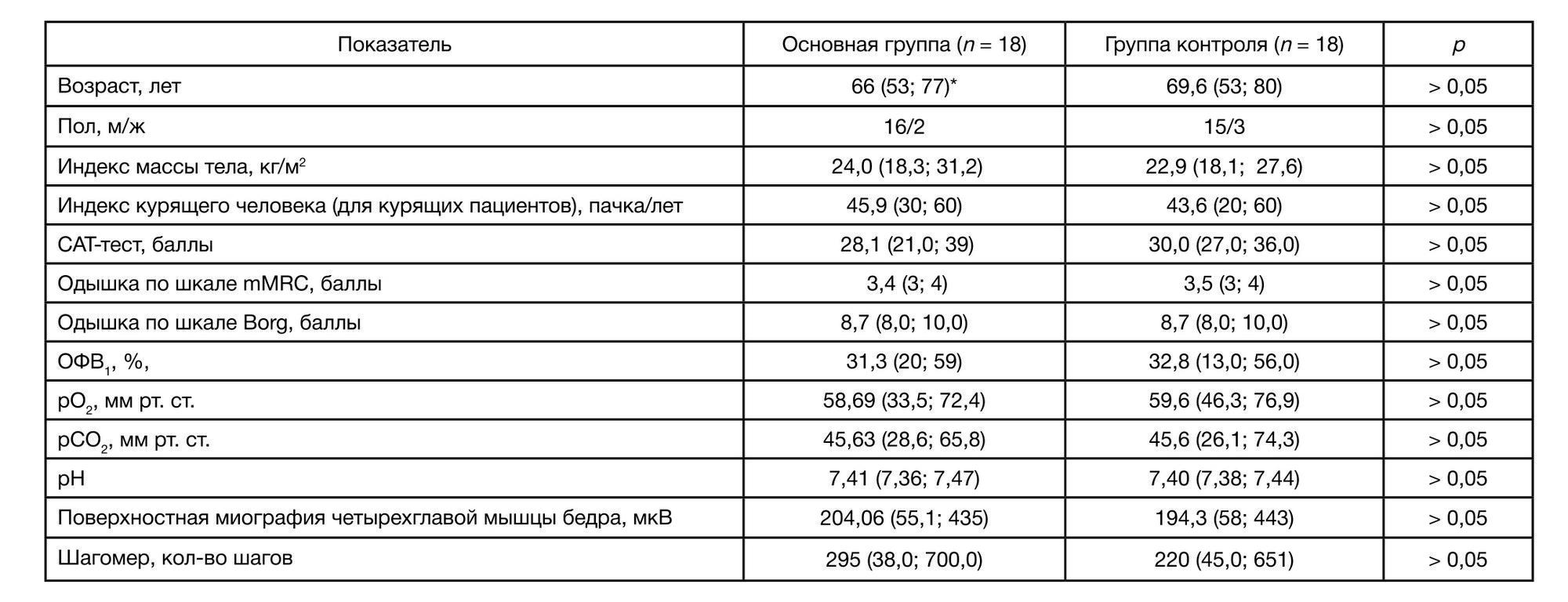
При поступлении пациенты обеих групп имели одинаковые основные характеристики, спирометрические данные и показатели миографии. Сравнение значений параметров ГАК (рН, PaO2, PaCO2) тоже не выявило существенной разницы (табл. 1).
Влияние электромиостимуляции на качество жизни
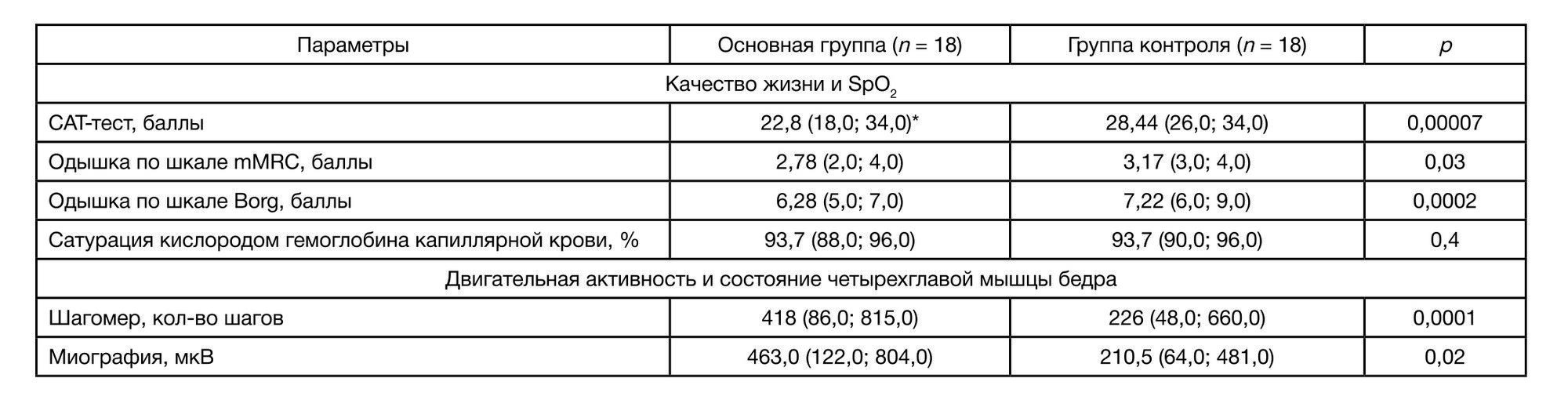
При анализе влияния ЭМС на качество жизни у пациентов основной группы выявлено улучшение показателей по САТ-тесту, шкале mMRC и шкале Borg. При этом в группе контроля значимого улучшения не выявлено (табл. 2).
Влияние электромиостимуляции на клинические показатели
Анализ влияния ЭМС на клинические параметры показал, что в обеих группах (основной и группе сравнения) заметно улучшились значения показателя SpO2, при этом на 10-й день в основной группе и группе сравнения достоверной разницы между значениями SpO2 не было установлено (табл. 2).
Влияние электромиостимуляции на двигательную активность и состояние четырехглавой мышцы бедра
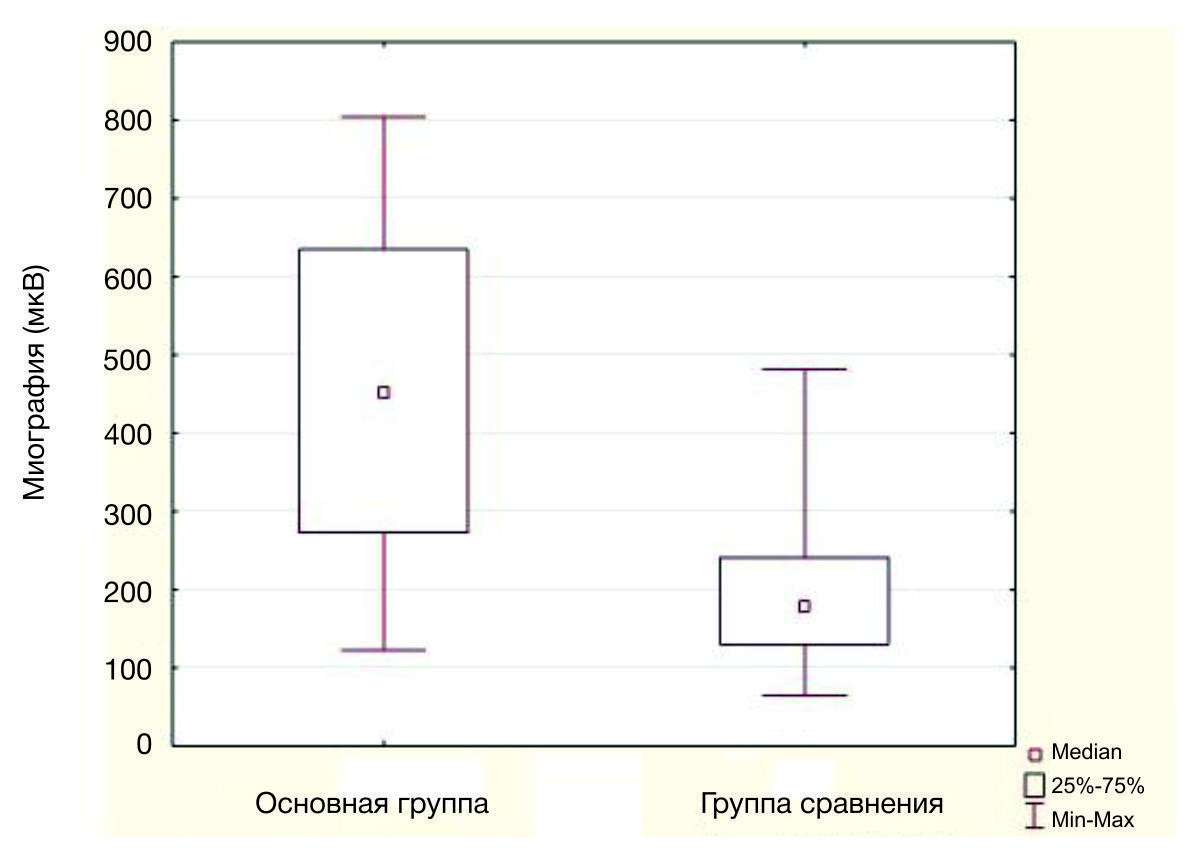
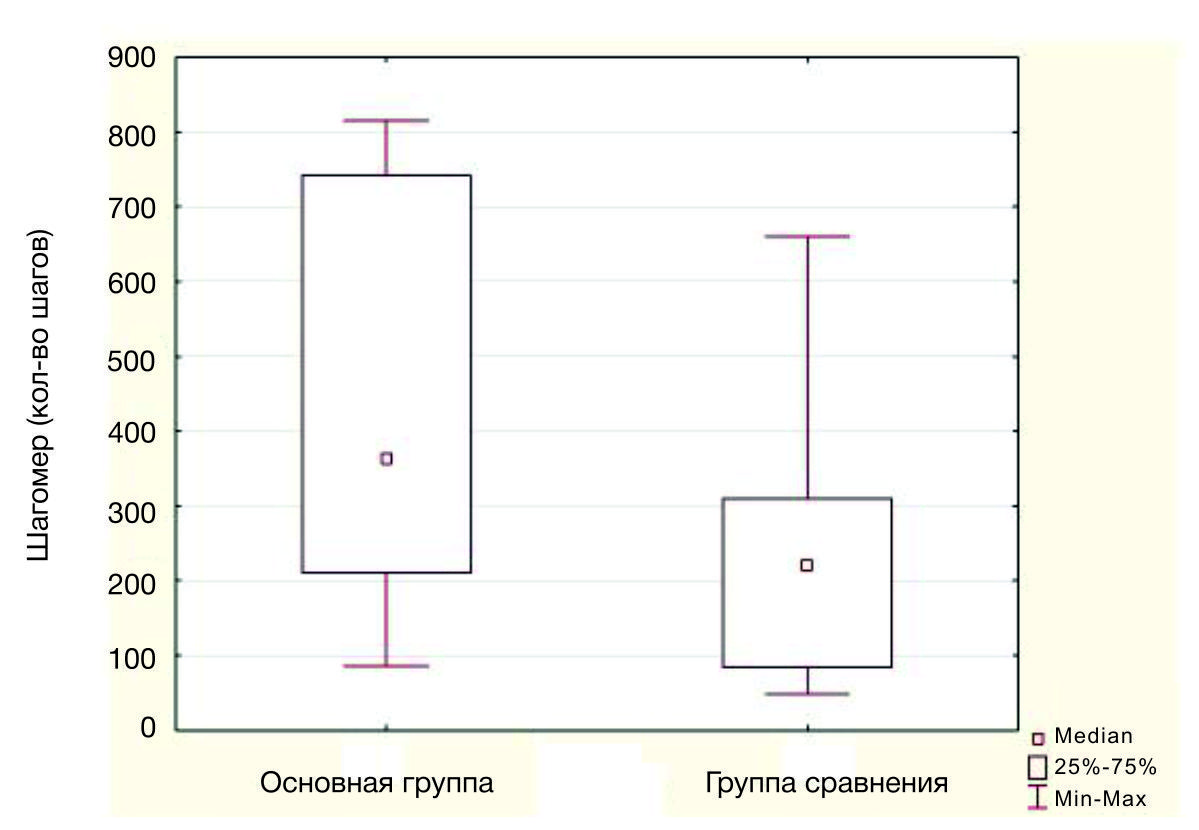
Внутригрупповой анализ показателей миографии и результатов измерений, сделанных шагомером, у пациентов основной группы показал их значительное улучшение. По результатам межгруппового анализа статистически значимое улучшение этих показателей наблюдалось у пациентов основной группы (рис. 2 и рис. 3 соответственно) на 10-й день (табл. 2).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Реабилитация пациентов с ХОБЛ имеет большое значение при комплексной терапии. Именно физическим тренировкам отводится при этом немаловажное значение. Эффективность легочной реабилитации у пациентов с ХОБЛ имеет большой уровень доказательности [2]. Однако встает вопрос о том, как помочь тем пациентам, которые не способны к выполнению стандартных программ легочной реабилитации. По литературным данным, альтернативой физическим упражнениям может стать метод электромиостимуляции.
К настоящему времени проведено небольшое число клинических исследований, посвященных изучению эффективности электромиостимуляции четырехглавой мышцы бедра как одного из вариантов легочной реабилитации пациентов с тяжелой и крайне тяжелой формами ХОБЛ [7–10]. В представленных работах электромиостимуляция проводилась в достаточно длительные сроки, около 4–6 недель, и имела положительный эффект [11–14]. В качестве оценки использовали преимущественно субъективные методы, такие как, шестиминутный тест, опросник святого Георгия [8]. Результаты нашего иссследования показывают, что электростимуляция четырехглавой мышцы бедра в короткие сроки тоже приводит к улучшению функции указанной мышцы. Наиболее достоверным критерием оценки эффективности электростимуляции являются результаты электромиографии. В нашей работе при оценке влияния электростимуляции на насыщение гемоглобина капиллярной крови кислородом отмечено повышение SpO2, как в основной группе, так и в группе сравнения, что, вероятнее всего, обусловлено параллельно проводимой терапией у данных пациентов: приемом бронхолитических препаратов, кислородотерапией, у отдельных пациентов респираторной поддержкой. При оценке влияния электростимуляции на субъективное состояние пациента, а именно при оценке результатов измерения одышки по шкале Borg во время физической нагрузки и шкале mMRC, показано достоверное улучшение самочувствия у пациентов основной группы, вероятно, за счет уменьшения одышки на фоне улучшения функциональных свойств скелетной мускулатуры. Кроме того, прослеживается достоверное уменьшение количества баллов по вопроснику САТ, что связано с повышением двигательной активности пациента и улучшением качества жизни [7].
В нашем исследовании все субъективные изменения подтверждаются достоверным улучшением показателей миографии и результатов измерений, сделанных шагомером, использовавшихся нами в качестве оценки эффективности.
ВЫВОДЫ
По результатам работы можно сделать вывод, что электромиостимуляция четырехглавой мышцы бедра может стать эффективной альтернативой тренировкам у больных с тяжелым обострением ХОБЛ. Данный метод можно использовать в качестве одного из компонентов программы легочной реабилитации у пациентов с ХОБЛ, не способных выполнять физические упражнения.
- Чучалин А. Г., Авдеев С. Н., Айсанов З. Р., Белевский А. С., Лещенко И. В., Мещерякова Н. Н., Овчаренко С. И., Шмелев Е. И. Федеральные клинические рекомендации по диагностике и лечению хронической обструктивной болезни легких. Пульмонология. 2014; (3): 15–54.
- Deckamer V, Vogelmeier C. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. Global Initiative for Chronic Obstructive Lung Disease. 2015: 1–44.
- Авдеев С. Системные эффекты у больных ХОБЛ. Врач. 2006; 12: 3–8.
- Перцева Т. А., Санина Н. А. Выраженность системных воспалительных реакций у больных хронической обструктивной болезнью легких. Пульмонология. 2013; (1): 38–41.
- Barreiro E, Gea J. Molecular and biological pathways of skeletal muscle dysfunction in chronic obstructive pulmonary disease. Chron Respir Dis. 2016; 13 (3): 297–311.
- Мухарлямов Ф. Ю., Сычева М. Г., Рассулова М. А., Разумов А. Н. Пульмонологическая реабилитация: современные программы и перспективы. Пульмонология. 2013; 6: 99–105.
- Ont Health Technol Assess Ser. Pulmonary Rehabilitation for Patients With Chronic Pulmonary Disease (COPD): an Evidence- Based Analysis.. 2012; 12 (6): 1–75
- Мещерякова Н. Н., Белевский А. С., Черняк А. В., Лебедин Ю. С. Влияние методов легочной реабилитации на маркеры системного воспаления и уровень тестостерона в крови у больных хронической обструктивной болезнью легких. Пульмонология. 2011; 2: 81–86.
- Rong-chang Chen, Xiao-ying Li. Effectivness of neuromuscular electrical stimulation for the rehabilitation of moderate-to-severe COPD: a meta-analysis. Chron Respir Dis. 2016; 13 (3): 297–311.
- Abdellaoui A, Préfaut C, Gouzi F, Couillard A, Coisy-Quivy M, Hugon G, et al. Skeletal muscle effects of electrostimulation after COPD exacerbation: a pilot study. Europ Resp J. 2011; 38: 781–8.
- Сандухадзе Б. Р. Возможности кардиосинхронизированной электромиостимуляции в лечении хронической сердечной недостаточности у больных на фоне ИБС [диссертация]. М.: 2009.
- Barreiro E, Gea J. Molecular and biological pathways of skeletal muscle dysfunction in chronic obstructive pulmonary disease. Chron Respir Dis. 2016; 13 (3): 297–311.
- Windholz T, Swanson T, Vanderbyl BL, Jagoe RT. The feasibility and acceptability of neuromuscular electrical stimulation to improve exercise performance in patients with advanced cancer: a pilot study. BMC Palliat Care. 2014; 13: 23.
- Fischer A, Spiegl M, Altmann K. Muscle mass, strength and functional outcomes in critically ill patients after cardiothoracic surgery: does neuromuscular electrical stimulation help? The Catastim 2 randomized controlled trial. Crit Care. 2015; 20: 30.
- Abdulai RM, Jensen TJ, Patel NR, Polkey MI, Jansson P, Celli BR, Rennard SI. Deterioration of Limb Muscle Function during Acute Exacerbation of Chronic Obstructive Pulmonary Disease. Am J Resp Crit Care Medicine. 2017; 197 (4): 433–49. DOI: 10.1164/rccm.201703-0615CI