ОРИГИНАЛЬНОЕ ИССЛЕДОВАНИЕ
Активация CD4+CD39+Т-клеток при колоректальном раке
1 Институт биологии, Карельский научный центр Российской академии наук (ИБ КарНЦ РАН), Петрозаводск
2 Республиканский онкологический диспансер, Петрозаводск
Патогенез колоректального рака (КРР) сопровождается значительными изменениями в состоянии иммунной системы. Однако роль аденозин-A2AR-опосредованного иммуносупрессорного механизма и в частности экспрессии молекулы эктонуклеозидтрифосфат-дифосфогидролазы-1 (ENTPD1), или CD39, в его развитии до конца не изучена. Целью работы было исследование роли СD4+ Т-клеток, прежде всего экспрессирующих CD39 регуляторных Т-лимфоцитов (Treg), в формировании иммунной супрессии при КРР, а также у больных острым панкреатитом (ОП). Экспрессию молекул лимфоцитами крови и опухоль-инфильтрирующими лимфоцитами (ОИЛ) анализировали методом проточной цитометрии. Содержание матричной РНК (мРНК) CD39 в лейкоцитах периферической крови определяли методом полимеразной цепной реакции (ПЦР) в реальном времени. В результате исследования показано, что у больных КРР накопление периферических CD4+CD39+ клеток происходит на поздних стадиях развития опухоли. Среди ОИЛ количество CD4+ Т-клеток, экспрессирующих молекулу CD39, выше, чем в крови тех же больных. Значительно повышен уровень экспрессии этой молекулы у регуляторных Т-клеток (Treg) больных КРР как на периферии, так и среди ОИЛ. Установлены достоверные связи между содержанием CD4+CD39+ T-клеток и показателями клеточного иммунитета больных КРР. Обнаружено, что уровень мРНК гена CD39 также увеличивался в процессе развития КРР. У больных ОП, напротив, содержание мРНК гена CD39 оставалось на уровне контроля, так же как и количество CD4+CD39+ Т-клеток в периферической крови. Таким образом, можно заключить, что активация CD4+CD39+ Т-клеток в процессе канцерогенеза играет важную роль и требует дальнейшего изучения.
Ключевые слова: колоректальный рак, эктонуклеотидаза CD39, Treg-клетки, транскрипционный фактор FOXP3
Финансирование: исследование выполнено в рамках государственного задания КарНЦ РАН, тема № 0221-2017-0043.
Для корреспонденции: Галина Анатольевна Жулай
ул. Пушкинская, д. 11, г. Петрозаводск, 185014; ur.xednay@111-ilaghz
Колоректальный рак (КРР) — одна из ведущих форм злокачественных новообразований среди онкологических заболеваний и причин смертности в России [1] и в мире [2, 3]. Число больных с первичным КРР постоянно растет, причем заболеваемость гораздо выше в индустриально развитых странах Европы и Северной Америки, чем в развивающихся странах Африки, Азии и Южной Америки [2]. Развитие КРР тесно связано с механизмами регуляции иммунного ответа и сопровождается инфильтрацией опухоли иммунокомпетентными клетками [3–5]. Активно обсуждается роль хронического воспаления как фактора, способствующего развитию КРР, так как у больных с воспалительными заболеваниями кишечника увеличен риск возникновения КРР. По некоторым данным, противовоспалительная терапия снижает вероятность развития опухолей желудочно-кишечного тракта [7, 8].
В настоящее время в онкоиммунологии уделяется значительное внимание изучению эктонуклеозидтрифосфат-дифосфогидролазы-1 (ENTPD1, CD39). Молекула CD39 совместно с CD73 (экто-5′-нуклеотидаза, NТ5E) участвует в генерации внеклеточного аденозина. Образование внеклеточных пуриновых нуклеозидов играет фундаментальную роль в регуляции воспаления и тканевого гомеостаза. В иммунокомпетентных клетках аденозин передает сигнал преимущественно через рецептор A2A (A2АR), один из четырех аденозиновых рецепторов, связанных с G-белком. Стимуляция A2АR лимфоцитов приводит к уменьшению секреции IL2 и пролиферативной активности нативных CD4+ Т-клеток; снижению уровня IFNγ и IL4 у Т-хелперов; увеличению экспрессии молекул CTLA-4, PD1 и CD40L [8]. Иммуносупрессорный механизм, включающий взаимодействие аденозина и A2АR, способен защищать нормальные ткани от повреждений при развитии воспалительных реакций. Однако этот сигнальный путь активируется и в опухолевой ткани, особенно в ответ на гипоксию, что обеспечивает защиту раковых клеток от распознавания иммунной системой и уничтожения [9]. Роль данного механизма в развитии опухолей была продемонстрирована на экспериментальных моделях А2АR–/–-мышей, у которых наблюдалась регрессия иммуногенных опухолей [10], а также мышей с нокаутом генов CD39 или CD73, отличающихся опухоль-резистентными свойствами [11, 12].
Экспрессия CD73 в опухолевой ткани описана довольно хорошо. Известно, что данный маркер экспрессируют различные типы клеток: опухолевые клетки, эндотелиальные клетки, клетки стромы [13]. Меньше известно об экспрессии в опухолевом микроокружении мембранного маркера СD39. Предполагается, что один из основных источников этой молекулы в инфильтрате опухоли — регуляторные Т-клетки (Treg) [14]. Используя различные супрессорные механизмы, Treg-клетки способны предотвращать развитие аутоиммунных реакций и поддерживать иммунологическую толерантность [15, 16]. Ключевым транскрипционным фактором этих клеток является FOXP3, который отвечает за их развитие и супрессорную функцию [17]. При канцерогенезе Treg -клетки играют негативную роль, способствуя развитию опухоли. Показано, что они присутствуют в большом количестве в периферической крови онкологических больных и ткани различных форм опухолей [18].
На сегодняшний день КРР — один из наиболее распространенных типов злокачественных новообразований, однако роль аденозин-A2AR иммуносупрессорного механизма в его развитии до конца не изучена. Поэтому целью работы было исследование роли СD4+ Т-клеток, экспрессирующих CD39, в формировании иммунной супрессии у больных КРР.
ПАЦИЕНТЫ И МЕТОДЫ
В работе обследовано 42 пациента с КРР, средний возраст которых составил 65 ± 12,4 лет. Критериями включения в исследование были: возраст 18–70 лет, наличие гистологически и цитологически подтвержденного диагноза «колоректальный рак». Критерии исключения: наличие других форм новообразований в анамнезе, а также иммуновоспалительных заболеваний. В качестве контроля анализировали лимфоциты 30 здоровых доноров в возрасте 54,4 ± 20,6 лет. Диагноз КРР устанавливался на основании клинических, лабораторных, эндоскопических и морфологических методов исследования. Было диагностировано 6 человек с I стадией КРР (14,3%), 15 — с II (37%), 12 — с III (28,6%) и 9 больных с IV стадией (20%). Пациенты были разделены на две группы: в первую группу входили больные на I и II стадиях КРР, во вторую — на III и IV стадиях. Для проведения исследования было получено разрешение Комитета по медицинской этике при Министерстве здравоохранения и социального развития Республики Карелия и Петрозаводском государственном университете (протокол № 25 от 12.02.2013 г.). Проведен анализ фенотипов клеток периферической крови, а также опухоль-инфильтрирующих лимфоцитов (ОИЛ), выделенных из клинических образцов опухолевой ткани (n = 5) больных с III стадией КРР.
Накопление аденозина в межклеточном пространстве происходит в ответ на метаболический стресс и разрушение клетки, т. е. при ишемии, гипоксии, воспалении и травме. В связи с этим интерес представляет исследование активации CD4+CD39+ клеток в условиях развития воспаления и иммунной супрессии, не связанной с канцерогенезом. В качестве такой группы сравнения были обследованы больные острым панкреатитом (ОП). В эту группу вошли 29 человек в возрасте 44,5 ± 18 лет. Диагноз был поставлен на основе классификации, принятой на IX Всероссийском съезде хирургов в 2000 г. Критериями включения в исследование, были: возраст 18–70 лет, наличие диагноза «острый панкреатит». Критерии исключения: наличие в анамнезе других нозологий, прежде всего новообразований, а также аутоиммунных патологий. Анализ лимфоцитов у больных КРР и ОП проводили до начала терапии.
Процедуру выделения ОИЛ выполняли методом ферментативной дезагрегации. Свежевыделенную ткань измельчали, переносили в среду для ферментативной дезагрегации и инкубировали при постоянном перемешивании в течение 2–3 ч при комнатной температуре. Среду готовили на основе RPMI-1640 (ПанЭко, Россия) с добавлением 10% FBS (HyClone, США), 100 мкг/мл гентамицина (Sigma, США) и 1 мг/мл коллагеназы IV (ПанЭко, Россия). Полученную суспензию пропускали через стерильные фильтры для клеток 70 и 40 мкм. Выделение фракции лимфоцитов проводили на раздельном градиенте фиколла в 75% и 100%, который готовили из фиколл плотностью 1,077 г/см3 (ПанЭко, Россия).
Экспрессию молекул клетками оценивали методом многоцветной проточной цитометрии на приборе Cytomics FC500 (Beckman Coulter, США) с использованием моноклональных антител CD4-FITC, CD8-FITC, CD25-PC5, CD127-PC7 (Beckman Coulter, Франция), CD3-PE, CD16- FITC, CD19-FITC (Сорбент, Россия), FOXP3-PE (eBioscience, США), CD39 (R&DSystems, США) и соответствующих изотипических контролей. Анализ внутриклеточной экспрессии FOXP3 выполняли с применением набора буферов для фиксации и пермеабилизации (eBioscience, США). Экспрессию мРНК CD39 определяли методом ПЦР в реальном времени. Выделение и очистку нуклеиновых кислот проводили с помощью набора «AxyPrep Blood Total RNA Miniprep Kit» (Axygen, США). Для синтеза кДНК использовали случайные гексапраймеры и MMLV-обратную транскриптазу (Силекс, Россия). Амплификацию кДНК, а также анализ продуктов амплификации в режиме реального времени выполняли с использованием реакционной смеси с интеркалирующим красителем SYBR Green I (Евроген, Россия) на приборе «iCycler Thermal Cycler» (Bio-Rad, США). Анализ полученных данных проводили методом 2–∆∆Ct, где Сt — пороговый цикл, а ∆Сt — разница между значениями пороговых циклов для референсного (GAPDH) и таргетного (CD39) генов. Итоговый уровень экспрессии исследуемого гена рассчитывали относительно контроля (здоровые доноры), принимая за единицу величину экспрессии исследуемого гена в контроле. Статистическую обработку данных проводили с использованием пакета программ «Statistica 6.0», достоверность различий между группами рассчитывали по критерию Манна–Уитни при уровне значимости р < 0,05. Для выявления и оценки характера связи между признаками использовали коэффициент ранговой корреляции Спирмена. Данные представлены в виде M ± SD. Исследование выполнено на научном оборудовании «Центра коллективного пользования Федерального исследовательского центра «Карельский научный центр Российской академии наук» (ЦКП КарНЦ РАН).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
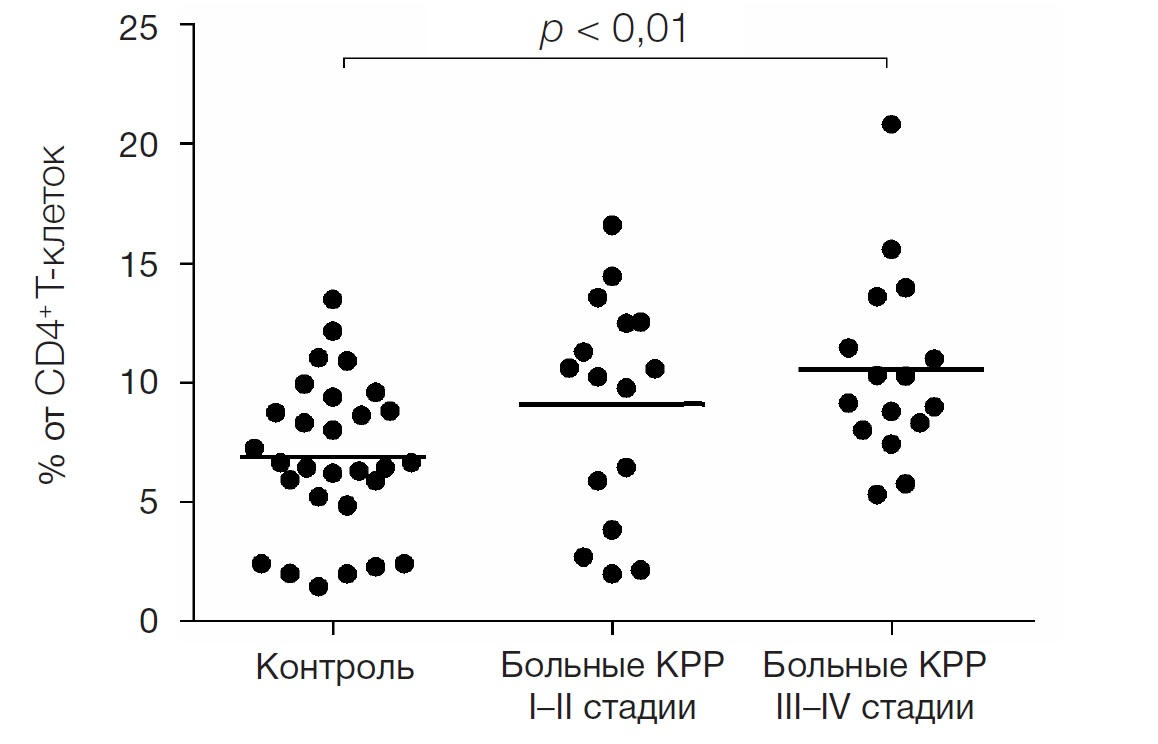
В работе определяли содержание CD4+CD39+ Т-клеток в периферической крови и среди ОИЛ у больных КРР. Обнаружено, что количество CD4+CD39+ T-клеток на периферии как у здоровых, так и у больных лиц сильно варьирует. При КРР на поздних стадиях содержание CD4+CD39+ лимфоцитов было выше, чем в контроле (p < 0,05). В то же время у больных с I и II стадиями КРР значительных отличий в содержании CD4+CD39+ клеток не отмечено (рис. 1).
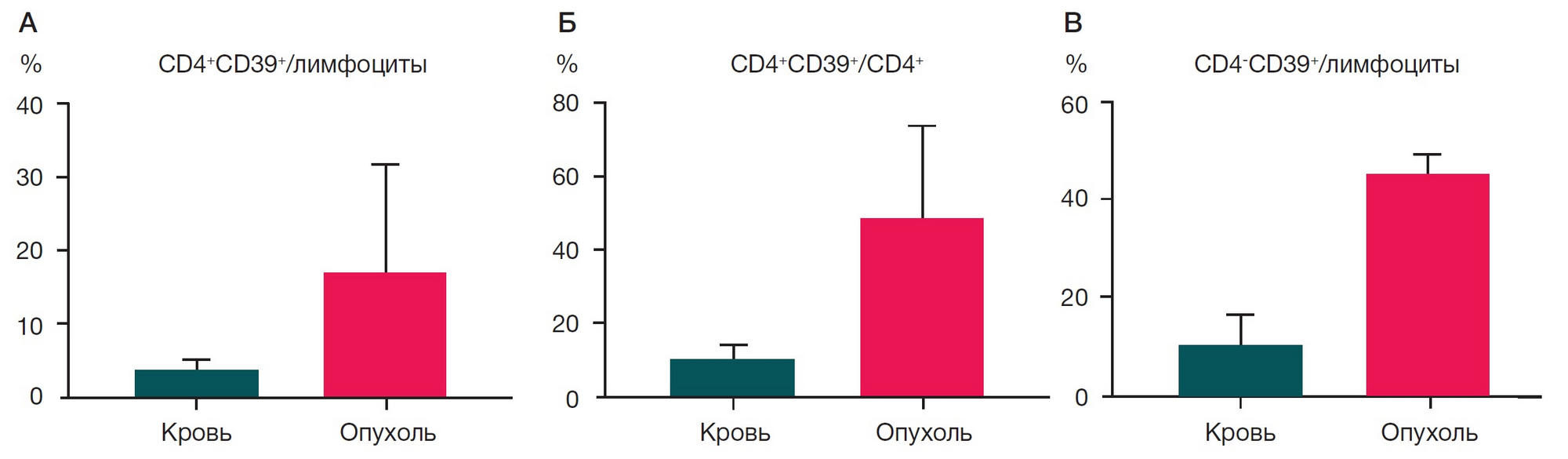
В опухолевой ткани среди лимфоцитов количество CD4+CD39+ Т-клеток было в 4 раза выше, чем в периферической крови тех же больных (рис. 2А).
Повышенное содержание CD4+CD39+ Т-клеток было отмечено и среди CD4+ Т-лимфоцитов (рис. 2Б). Также увеличенное количество CD39+ клеток среди ОИЛ наблюдалось в популяции Т-клеток, не несущих на своей поверхности CD4 (рис. 2В). При этом в опухолевой ткани доля СD4–CD39+ клеток была больше, чем CD4+CD39+ (p < 0,05), чего не отмечено среди лимфоцитов, циркулирующих в крови.
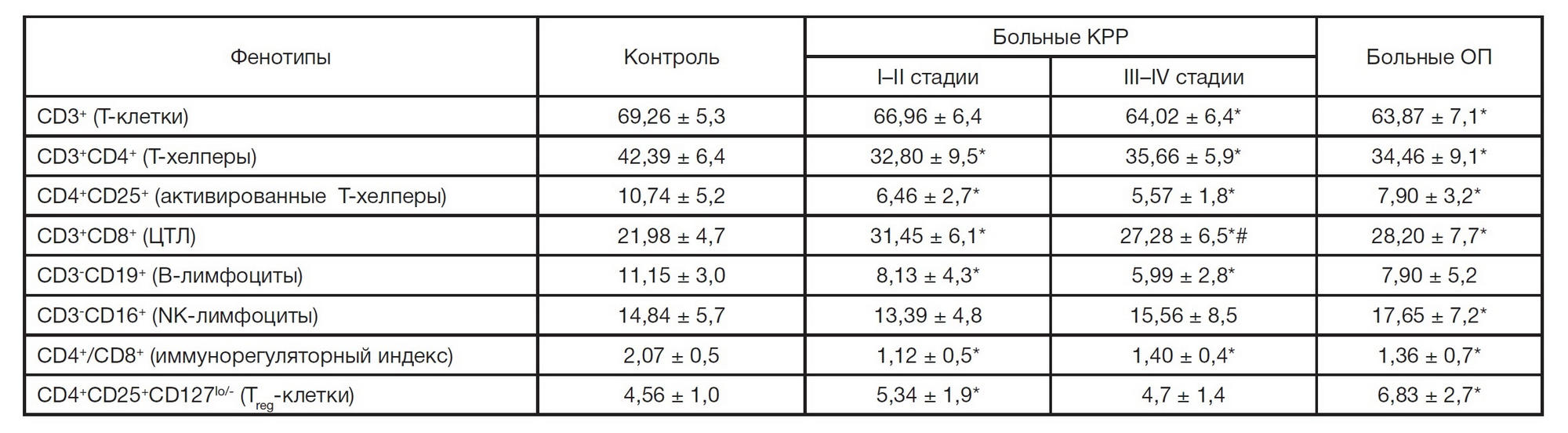
Ранее мы исследовали у больных КРР популяционный состав периферических лимфоцитов (Т-клетки и их субпопуляции, В-клетки и NK-клетки, или естественные киллеры) [19]. Результаты цитометрического анализа представлены в табл. 1.
У больных КРР по сравнению с контролем снижено число В-лимфоцитов, как на начальных стадиях развития заболевания, так и на поздних (p < 0,05). Изменения количества CD3+ Т-лимфоцитов отмечены для больных с III–IV стадиями КРР. На всех стадиях развития КРР наблюдалось пониженное число CD4+ Т-хелперов (p < 0,05) и активированных CD4+CD25+ Т-клеток (p < 0,05), а также повышенное количество CD8+ цитотоксических лимфоцитов (ЦТЛ, p < 0,05). У больных КРР в уровне NK-клеток достоверных различий по сравнению с контролем не выявлено.
Мы выявили связь изменений в популяционном составе лимфоцитов с количеством CD4+CD39+ Т-клеток у больных КРР. Отмечена отрицательная корреляция между количеством CD3+CD4+ T-хелперов и CD4+CD39+ T-клеток (r = –0,60, p < 0,05), между количеством CD3–CD19+ В-клеток и CD4+CD39+ T-клеток (r = –0,40, p < 0,05), а также между значением иммунорегуляторного индекса (отношение клеток CD4+/CD8+) и количеством CD4+CD39+ T-клеток (r = –0,58, p < 0,05). Полученные данные свидетельствуют об участии CD4+CD39+ T-клеток в иммуносупрессии при развитии КРР.
Важную роль при канцерогенезе играет субпопуляция Treg-клеток. Кроме того, экспрессия Treg -клетками молекулы CD39 и участие в генерации внеклеточного аденозина рассматривается как один из основных механизмов супрессии иммунного ответа [15, 16]. Мы исследовали содержание Treg -клеток с фенотипом CD4+CD25+CD127lo/–. У больных с I–II стадиями КРР количество CD4+CD25+CD127lo/– Treg-клеток было увеличено по сравнению со здоровыми донорами, тогда как у больных на поздних стадиях КРР количество этих клеток не отличалось от контроля (табл. 1). Было показано, что в крови онкологических больных на Treg-клетках (CD4+CD25+CD127lo/–, CD4+CD25+) происходит усиление уровня экспрессии молекулы CD39 (табл. 2).
Как видно из табл. 2, экспрессия CD39 у CD4+CD25+CD127lo/– Treg -клеток увеличивается уже на начальных этапах (I–II стадии) развития опухоли по сравнению с контролем и достигает максимальных значений у больных с более поздними стадиями КРР. Такая же закономерность наблюдалась и для CD4+CD25+ Treg-клеток. Тогда как у клеток с фенотипом CD4+CD25– уровень экспрессии CD39 был довольно низким и не отличался от контроля.
Кроме того, в данной работе исследовали экспрессию транскрипционного фактора Treg-клеток FOXP3 и ее связь с экспрессией CD39. Показано, что между экспрессией CD39 и экспрессией FOXP3 в CD4+CD25+ Т-клетках в крови больных КРР существует прямая корреляция (r = 0,51, p < 0,05). Среди ОИЛ CD4+CD25+ Treg -клетки также отличались от периферических более высокой экспрессией CD39. При этом почти все ОИЛ с фенотипом CD4+CD25+ экспрессировали маркер CD39 (табл. 2). Однако повышенная экспрессия этой молекулы наблюдалась и у нерегуляторных клеток с фенотипом CD4+CD25– по сравнению с периферическими лимфоцитами этих же больных. Полученные данные свидетельствуют о том, что опухоль стимулирует экспрессию CD39 на различных субпопуляциях CD4+ Т-лимфоцитов, включая Treg -клетки.
Исследование изменения субпопуляционного состава лимфоцитов и относительного количества Treg-клеток проводили и у больных ОП (табл. 1). Содержание Т-лимфоцитов и CD4+ Т-клеток, а также количество активированных Т-хелперов у больных ОП было ниже, чем в контроле. Однако уровень экспрессии CD25 в Т-хелперах больных ОП был выше, чем в контроле (25,37 ± 8,6% и 18,09 ± 7,5% от числа CD4+ T-клеток соответственно, p < 0,05). Изменения в соотношении субпопуляций Т-клеток отразились в значительном снижении иммунорегуляторного индекса (ИРИ). Показано, что у больных ОП увеличено содержание CD8+ ЦТЛ и NK-клеток по сравнению со здоровыми донорами. Таким образом, больные ОП, так же как больные КРР проявляли признаки ослабления иммунитета. Кроме того, было обнаружено, что у больных ОП число периферических CD4+CD25+CD127lo/– Treg-клеток выше, чем в контроле (табл. 1).
В результате исследования экспрессии молекулы эктонуклеотидазы CD39 было обнаружено, что у больных ОП количество CD4+CD39+ T-клеток составило 9,16 ± 2,9% от CD4+ Т-клеток. Показано, что в уровне экспрессии CD39 Treg-клетками больных ОП наблюдалась схожая с КРР закономерность. Экспрессия этой молекулы была выше в Treg-клетках (p < 0,05) у больных ОП. Так, уровень экспрессии CD39 Treg-клетками с фенотипом CD4+CD25+ у больных ОП составил 57,98 ± 19,6%, тогда как в CD4+CD25+CD127lo/– Treg-клетках — 62,09 ± 16,4%. У CD4+CD25– лимфоцитов, не относящихся к Treg-клеткам, уровень экспрессии CD39 составил 7,67 ± 4,3%, достоверных отличий от контроля не выявлено.
Как и при КРР, мы исследовали степень вовлеченности популяции CD4+CD39+ T-клеток в иммунную супрессию больных ОП. Однако в результате корреляционного анализа содержания CD4+CD39+ T-клеток, уровня экспрессии этой молекулы в CD4+CD25+CD127lo/– Treg -клетках и количественных изменений в популяционном составе лимфоцитов больных ОП не выявили ни одной достоверной связи, как это было при КРР.
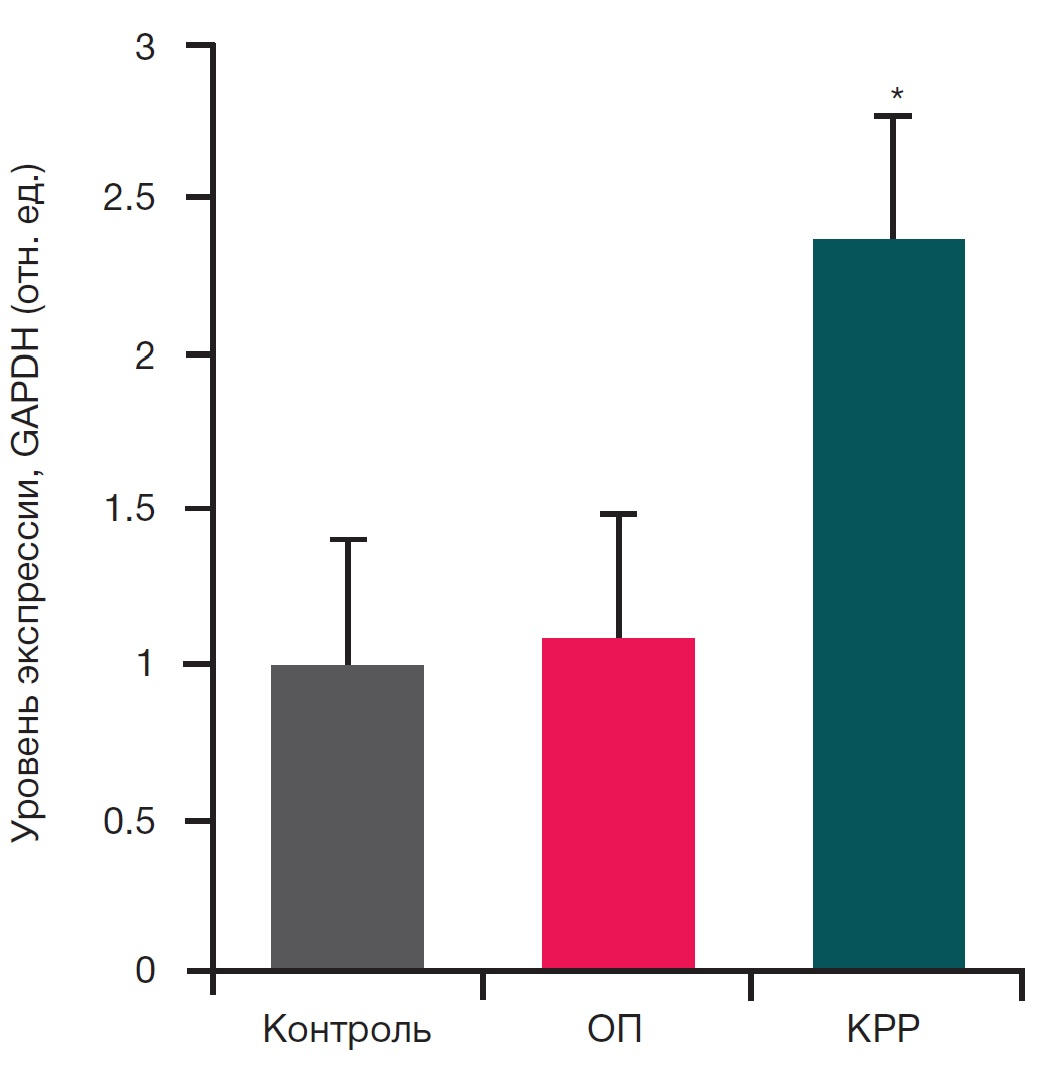
Кроме того, нами был исследован относительный уровень экспрессии мРНК гена CD39 в лейкоцитах периферической крови больных КРР и ОП. Обнаружено, что у больных КРР уровень мРНК этого гена был в 2,36 раза выше, чем в контроле (рис. 3). У больных ОП не было выявлено существенных отличий в уровне экспрессии транскриптов CD39.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Внеклеточный аденозин — сигнальная молекула, модулирующая многие физиологические процессы. В последнее время активно исследуется аденозин- опосредованная супрессия иммунного ответа как один из ключевых механизмов резистентности опухоли к иммунологическому надзору. Образуется аденозин дефосфорилированием аденозинмонофосфата (АМФ) в межклеточном пространстве. Одним из ключевых ферментов в этом процессе служит эктонуклеотидаза CD39, обеспечивающая превращение аденозинтрифосфата (АТФ) и аденозиндифосфата (АДФ) до АМФ [8, 9].
В настоящей работе исследовали роль СD4+ Т-клеток, экспрессирующих CD39, в формировании иммунной супрессии у больных КРР. Нами было показано, что у больных КРР накопление периферических CD4+CD39+ клеток происходит на поздних стадиях развития опухоли. Среди ОИЛ количество CD4+ Т-клеток, экспрессирующих молекулу CD39, значительно выше, чем в крови тех же больных. Кроме того, у обследованных онкологических больных существует отрицательная корреляция между содержанием CD4+CD39+ T-клеток и другими показателями, такими как количество CD3+CD4+ T-хелперов, CD3–CD19+ В-клеток и значение ИРИ, что свидетельствует об участии CD4+CD39+ T-клеток в иммуносупрессии при развитии КРР.
Важную роль в формировании иммунной супрессии при канцерогенезе и поддержании опухолевого роста отводят популяции Treg-клеток. Недавно было продемонстрировано, что Тreg-клетки могут участвовать в накоплении внеклеточного аденозина. Они отличаются от других Т-лимфоцитов повышенной экспрессией молекулы CD39, необходимой для супрессорной активности этих клеток [20, 21]. Было показано, что Treg-клетки, выделенные из крови CD39–/–-мышей проявляют низкий уровень супрессорной активности in vitro и не могут предотвращать отторжение трансплантата in vivo [22]. Поверхностная экспрессия CD73 (нуклеотидазы, дефосфорилирующей АМФ до аденозина) совместно с CD39 определяется у CD4+CD25+ Treg клеток мышей. У человека CD4+CD25+ Т-клетки обладают крайне низким уровнем экспрессии CD73 [23], но при этом уровень экспрессии CD73 в цитоплазме этих клеток выше по сравнению с CD4+CD25– Т-лимфоцитами [21]. Более того, было продемонстрировано прямое накопление аденозина в культуре Treg-клеток человека, подтверждающее, что в этих клетках CD73 присутствует в активной форме.
В нашей работе показано, что в крови больных КРР уровень экспрессии маркера CD39 в клетках с фенотипами CD4+CD25+ и CD4+CD25+CD127lo/– был значительно выше у всех обследованных больных. При этом усиление экспрессии эктонуклеотидазы зависело от стадии заболевания. Среди ОИЛ CD4+CD25+ Treg-клетки также отличались от периферических более высокой экспрессией этой молекулы. Таким образом, можно заключить, что в результате процесса рекрутинга из периферического пула лимфоцитов, среди ОИЛ происходит накопление Treg-клеток с высокой экспрессией CD39+. Эти клетки являются одной из доминирующих субпопуляций Treg при развитии КРР, особенно на более поздних стадиях заболевания. Кроме того, CD39+ Treg-клетки отличает более высокая иммуносупрессорная активность, что может оказывать негативный эффект при развитии заболевания наряду с другими механизмами иммунной супрессии.
Развитие ОП, особенно в деструктивной форме, тоже сопровождается изменением реактивности иммунной системы. Это заболевание характеризуется воспалением поджелудочной железы с возможным вовлечением перипанкреатических тканей и формированием полиорганной функциональной недостаточности, которая в свою очередь возникает в следствие панкреонекроза, развития инфекции и сепсиса [24]. Предполагается, что выраженность иммунных характеристик синдрома системного воспалительного ответа может индуцировать развитие иммуносупрессии, что приводит к неспособности организма противостоять микробной агрессии и, как следствие, к развитию гнойно- некротических осложнений [25].
Полученные нами данные об изменениях в субпопуляционном составе лимфоцитов, повышенном содержании Treg-клеток у больных ОП могут свидетельствовать о развитии иммунной супрессии при данном заболевании. Учитывая повышенное содержание Treg-клеток, а также воспалительный характер заболевания и увеличение уровня апоптоза циркулирующих лимфоцитов [26], предполагается, что развитие иммунной супрессии у таких больных представляет компенсаторный механизм, ограничивающий развитие воспалительной реакции.
В отличие от пациентов с КРР, у больных ОП содержание CD4+CD39+ клеток не отличалось от контроля. Не выявлено корреляции между содержанием основных популяций лимфоцитов и уровнем CD4+CD39+ T-клеток. Отмечено, что у больных ОП был увеличен уровень экспрессии CD39 на Treg-клетках (CD4+CD25+ и CD4+CD25+CD127lo/–) по сравнению с контролем, что, возможно, связано с повышенным количеством самих Treg-клеток в крови этих больных. По-видимому, у больных ОП CD4+СD39+ Т-клетки не вносят значительного вклада в развитие системной иммуносупрессии, как при канцерогенезе. Об этом также свидетельствуют полученные нами результаты анализа относительного уровня мРНК гена CD39 у больных КРР и ОП. Было показано, что у больных КРР уровень мРНК CD39 увеличивался в процессе развития заболевания, достигая максимальных значений на поздних стадиях КРР. В то же время, у больных ОП уровень экспрессии CD39 не отличался от контроля.
ВЫВОДЫ
В условиях развития КРР значительно повышается количество CD4+ Т-клеток, экспрессирующих маркер CD39, особенно интенсивное накопление CD39+ клеток наблюдается среди ОИЛ. Эти клетки играют существенную роль в формировании иммунной супрессии у больных КРР. Значительную долю клеток, экспрессирующих CD39, составляют Treg-лимфоциты. Блокировка экспрессии эктонуклеотидазы CD39 и/или ограничение функционирования Treg-клеток представляет интерес для разработки новых подходов к противоопухолевой терапии. Необходимы дальнейшие исследования для детального понимания механизмов аденозин-А2АR-опосредованной иммунной супрессии у онкологических больных.

- Каприн А. Д., Старинский В. В., Петрова Г. В., редакторы. Состояние онкологической помощи населению России в 2015. М.: МНИОИ им. Герцена; 2016. 250 с.
- Циммерман Я. С. Колоректальный рак: современное состояние проблемы. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2012; 22 (4): 5–17.
- Mougiakakos D. Regulatory T cells in colorectal cancer: from biology to prognostic relevance. Cancers. 2011; 3: 1708–31.
- Salama P, Phillips M, Grieu F, Morris M, Zeps N, Joseph D, et al. Tumor-infiltrating FOXP3+ T regulatory cells show strong prognostic significance in colorectal cancer. J. Clin. Oncol. 2009; 27: 186–92.
- Nosho K, Baba Y, Tanaka N, Shima K, Hayashi M, Meyerhardt JA, et al. Tumour-infiltrating T-cell subsets, molecular changes in colorectal cancer, and prognosis: cohort study and literature review. J Pathol. 2010; 222 (4): 4350–66.
- Lutgens MW, Vleggaar FP, Schipper ME, Stokkers PC, van der Woude CJ, Hommes DW, et al. High frequency of early colorectal cancer in inflammatory bowel disease. Gut. 2008; 57: 1246–51.
- Lasry A, Zinger A, Ben-Neriah Y. Inflammatory networks underlying colorectal cancer. Nat Immunol. 2016; 17 (3): 230–40.
- Antonioli L, Blandizzi C, Pacher P, Haskó G. Immunity, inflammation and cancer: a leading role for adenosine. Nat Rev Cancer. 2013; 13: 842–57.
- Antonioli L, Pacher P, Vizi ES, Haskó G. CD39 and CD73 in immunity and inflammation. Trends Mol Med. 2013; 19: 355–67.
- Sitkovsky MV, Kjaergaard J, Lukashev D, Ohta A. Hypoxia-adenosinergic immunosuppression: tumor protection by T regulatory cells and cancerous tissue hypoxia. Clin Cancer Res. 2008; 14: 5947–52.
- Jackson SW, Hoshi T, Wu Y, Sun X, Enjyoji K, Cszimadia E, et al. Disordered purinergic signaling inhibits pathological angiogenesis in cd39/Entpd1-null mice. Am J Pathol. 2007; 171: 1395–404.
- Stagg J, Beavis PA, Divisekera U, Liu MC, Moller A, Darcy PK, et al. CD73-deficient mice are resistant to carcinogenesis. Cancer Res. 2012; 72: 2190–6.
- Beavis PA, Stagg J, Darcy PK, Smyth MJ. CD73: a potent suppressor of antitumor immune responses. Trends Immunol. 2012; 33: 231–7.
- Bastid J, Cottalorda-Regairaz A, Alberici G, Bonnefoy N, Eliaou JF, Bensussan A. ENTPD1/CD39 is a promising therapeutic target in oncology. Oncogene. 2013; 32: 1743–51.
- Кравченко П. Н., Жулай Г. А., Чуров А. В., Олейник Е. К., Олейник В. М., Барышева О. Ю. И др. Субпопуляции регуляторных Т-лимфоцитов в периферической крови больных ревматоидным артритом. Вестник РАМН. 2016; 71(2): 148–153.
- Чуров А. В. Регуляторные Т-клетки и старение организма. Успехи геронтологии. 2013; 26 (4): 603–609.
- Morikawa H, Sakaguchi S. Genetic and epigenetic basis of Treg cell development and function: from a FoxP3-centered view to an epigenome-defined view of natural Treg cells. Immunological Reviews. 2014; 259 (1): 192–205.
- Whiteside TL. Regulatory T cell subsets in human cancer: are they regulating for or against tumor progression? Cancer Immunol Immunother. 2014; 63: 67–72.
- Жулай Г. А., Олейник Е. К., Романов А. А., Олейник В. М., Чуров А. В., Кравченко П. Н. Циркулирующие регуляторные Т-клетки и изменения в субпопуляционном составе лимфоцитов у больных колоректальным раком. Вопросы онкологии. 2016; 62 (1): 96–100.
- Deaglio S, Dwyer KM, Gao W, Friedman D, Usheva A, Erat A, et al. Adenosine generation catalyzed by CD39 and CD73 expressed on regulatory T cells mediates immune suppression. J Exp Med. 2007; 204: 1257–65.
- Mandapathil M, Hilldorfer B, Szczepanski MJ, Czystowska M, Szajnik M, Ren J, et al. Generation and accumulation of immunosuppressive adenosine by human CD4+CD25highFOXP3+ regulatory T cells. Journal of Biological Chemistry. 2010; 285: 7176–86.
- Ernst PB, Garrison JC, Thompson LF. Much ado about adenosine: adenosine synthesis and function in regulatory T cell biology. J Immunol. 2010; 185: 1993–98.
- Dwyer KM, Deaglio S, Gao W, Friedman D, Strom TB, Robson SC. CD39 and control of cellular immune responses. Purinergic Signal. 2007; 3: 171–80.
- Al Mofleh IA. Severe acute pancreatitis: pathogenetic aspects and prognostic factors. World J Gastroenterol. 2008; 14: 675–84.
- Винник Ю. С., Черданцев Д. В., Салмина А. Б., Маркелова Н. М., Миллер С. В. Особенности регуляции апоптоза иммунокомпетентных клеток крови при остром деструктивном панкреатите. Новости хирургии. 2011; 9 (2): 37–42.
- Zhang XP, Chen HQ, Liu F, Zhang J. Advances in researches on the immune dysregulation and therapy of severe acute pancreatitis. J Zhejiang Univ Sci B. 2009; 10 (7): 493–8.