ОРИГИНАЛЬНОЕ ИССЛЕДОВАНИЕ
Катаболиты триптофана и гены ферментов микробиома кишечника
1 Российский национальный исследовательский медицинский университет имени Н. И. Пирогова, Москва, Россия
2 Российский университет дружбы народов имени Патриса Лумумбы, Москва, Россия
3 Центр цифровой и трансляционной биомедицины ООО «Центр молекулярного здоровья», Москва
4 Институт фундаментальной медицины и биологии Казанского (Приволжского) федерального университета, Казань, Россия
5 Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева, Москва, Россия
6 Центр стратегического планирования и управления медико-биологическими рисками здоровью Федерального медико-биологического агентства, Москва, Россия
7 Национальный медицинский исследовательский центр эндокринологии, Москва, Россия
Общеизвестна сигнальная роль триптофана и его катаболитов. Однако до сих пор не изучено их влияние на потенциальную метаболическую активность микробиоты. Целью исследования было провести анализ согласованности изменений прогностической представленности генов ферментов микробиома кишечника и катаболитов триптофана. В исследовании приняли участие 109 здоровых добровольцев и 114 больных с ожирением. Количественный анализ катаболитов обмена триптофана в кале проводили методом ВЭЖХ. Из образцов фекалий выделяли бактериальную ДНК и проводили секвенирование (V3-V4 региона) гена 16S рРНК. Первичную обработку данных секвенирования осуществляли в программе «QIIME v.1.9.1». Анализ предположительной метаболической роли участников микробиоты проводили путем реконструкции ненаблюдаемых состояний при помощи PICRUSt. Максимальное количество статистически значимых взаимосвязей между катаболитами триптофана и прогностической представленностью генов ферментов микробиома у лиц с ожирением было установлено для индол-3-лактата. Показана статистически значимая взаимосвязь индол-3-лактата и представленности генов ферментов обмена фруктозы, аминосахаров, нуклеотидов, аминокислот, полиаминов и сульфосахаров. Установлено, что у больных ожирением происходит трехкратное увеличение индол-3-лактат-продуцирующей микробиоты. Показано, что микробиотическая популяция кишечника представлена совершенно другими родами и видами микроорганизмов у лиц, имеющих ожирение. Сделан вывод, что при ожирении индол-3-лактат значимо влияет на прогностическую представленность генов ферментов микробиома кишечника.
Ключевые слова: микробиом кишечника, метаболиты обмена триптофана, индол-3-лактат, индол, микробные катаболиты триптофана (MICT)
Финансирование: работа выполнена в рамках договора № 0373100122119000041 по проекту «Создание банка биообразцов сыворотки крови и фекалий от здоровых доноров и пациентов с ожирением, метаболическим синдромом, сахарным диабетом II типа, нарушением мукозального барьера желудочно-кишечного тракта с целью выявления кандидатных видонеспецифических медиаторов систем quorum sensing микробиоты человека, модулирующих эндокринную и метаболическую функцию жировой ткани».
Вклад авторов: О. П. Шатова — сбор первичного материала, статистическая обработка, подготовка текста статьи и рисунков; А. М. Гапонов — подготовка текста статьи; Т. В. Григорьева — исследование микробиома; И. Ю. Васильев — исследование микробиома и статистическая обработка данных; Л. С. Столетова — анализ материала; В. В. Макаров, С. М. Юдин — написание разделов статьи; С. А. Румянцев — идея исследования, редактирование статьи; А. В. Шестопалов — идея исследования, анализ материала, написание и редактирование статьи.
Соблюдение этических стандартов: исследование одобрено этическим комитетом РНИМУ имени Н. И. Пирогова (протокол № 186 от 26 июня 2019 г.). Все пациенты подписали добровольное информированное согласие на использование биологического материала в научных целях.
Для корреспонденции: Ольга Петровна Шатова
ул. Островитянова, д. 1, г. Москва, 117997; moc.liamg@po.avotahs
В последнее десятилетие исследования, направленные на понимание роли хологенома, вышли на новый уровень благодаря достижениям в области высокопроизводительного секвенирования следующего поколения (NGS), которые помогли точно идентифицировать виды микроорганизмов и связанные с ними метаболические пути. Хологеном описывает генетическую совокупность генов-хозяина и симбиотических/мутуалистических микробных генов [1]. Опубликовано множество работ по изучению таксономической представленности микробиоты кишечника при различных физиологических и патологических состояниях. Многие исследователи уделяют пристальное внимание изучению роли дисбиоза при развитии ожирения и сахарного диабета [2], неспецифического язвенного колита [3] и других заболеваний кишечника [4–6]. Не вызывает сомнения тот факт, что микробиота кишечника является одним из основных игроков в развитии метаболических заболеваний и так называемого «метаболического воспаления» [7]. Известно, что метаболиты, образуемые микробиотой, выполняют роль сигнальных молекул [8]. Установлено, что индол-3-этанол, индол-3-пируват и индол-3-альдегид через арилуглеводородные рецепторы (AhR) энтероцитов регулируют целостность апикального соединительного комплекса и обеспечивают нормальную проницаемость кишечника [9, 10]. Таким образом, микробные метаболиты триптофана (MICT) модулируют барьерную функцию кишечника и устойчивость к кишечным патогенам [11]. Однако до сих пор мало данных о регуляции триптофановыми производными ферментов микробиоты кишечника. В связи с чем одной из задач нашего исследования было установить взаимосвязь прогностической представленности генов ферментов у кишечного микробиома с содержанием триптофановых катаболитов.
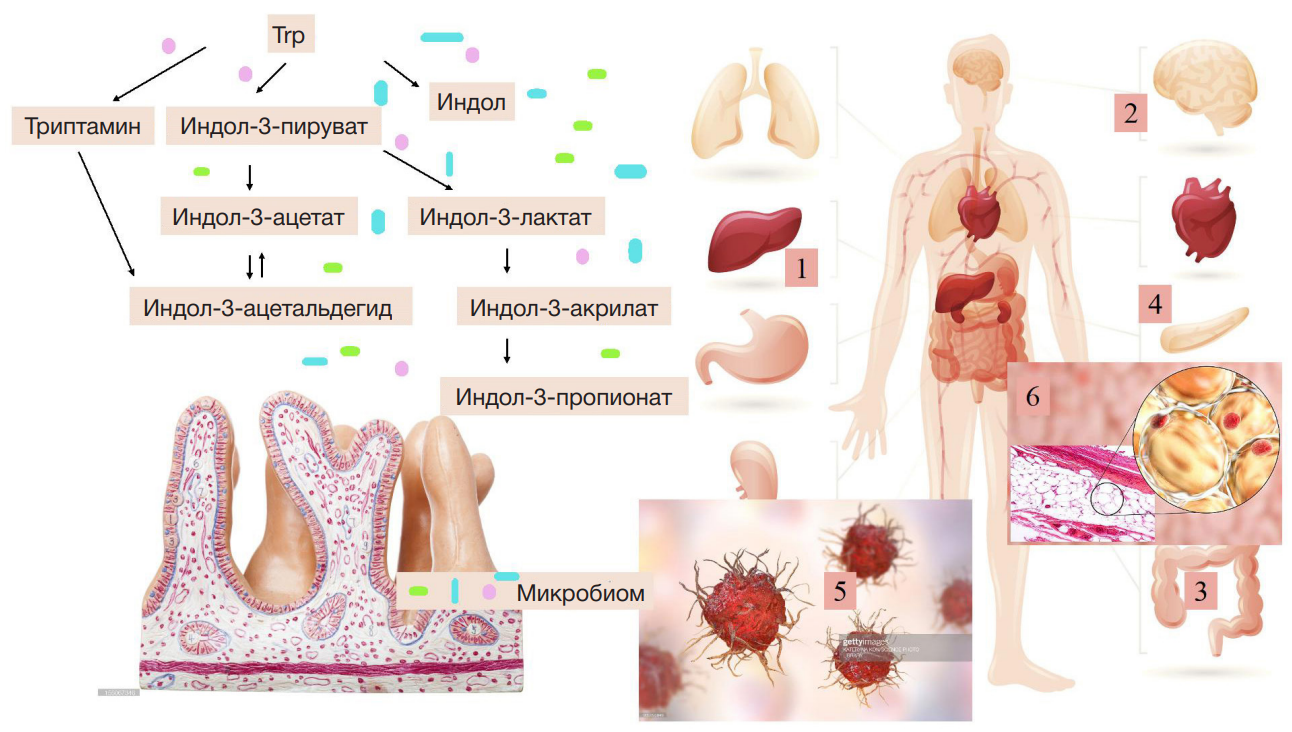
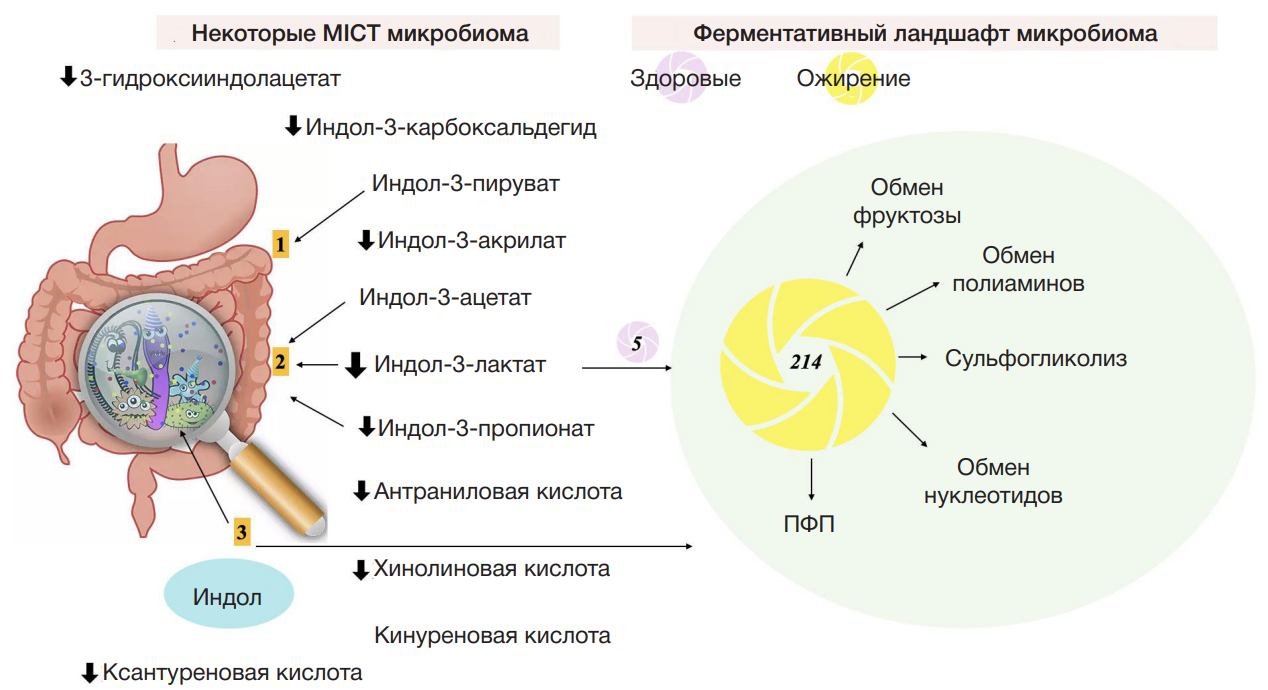
Многие исследователи проводят анализ особенностей таксономического состава микробиоты кишечника в норме и при различных патологиях [12, 13], включая ожирение, или изучают содержание катаболитов триптофана в кале, которые с большой вероятностью образуются исключительно микробиотой [8]. Однако все это еще предстоит доказать, так как состав микробиоты для больных с ожирением еще до конца не изучен [12]. Некоторые авторы считают индол-3-ацетат исключительно микробиотическим метаболитом [13], но при этом у человека экспрессируется фермент, который потенциально может образовывать данный метаболит. Это фермент, который превращает индол-3-ацетальдегид в индол-3-ацетат, — альдегиддегидрогеназа (ЕС: 1.2.1.3) [14]. В связи с чем второй задачей нашего исследования было оценить согласованность изменений содержания триптофановых метаболитов и ферментов, которые потенциально могут принимать участие в их продукции. В настоящее время принято считать, что к MICT относят: индол, триптамин, скатол, индол-3-пируват, индол-3-лактат, индол-3-акрилат, индол-3-пропионат, индол-3-ацетамид, индол-3-этанол, индол-3-альдегид и индол-3-ацетальдегид [8]. Необходимо отметить, что из всех MICT самая высокая концентрация в кишечнике установлена для индола, который является как молекулой quorum sensing (QS) микробиоты, так и сигнальной молекулой в организме человека [15]. К основным MICT общепринято также относить индол-3ацетат и индол-3-лактат [16]. Триптофан, получаемый из пищи, может метаболизироваться в индол-3-ацетат микробиотой кишечника через индол-3-ацетамидный путь при катализе триптофанмонооксигеназой (ЕС: 1.13.12.3) и индол-3-ацетамидгидролазой (ЕС: 3.5.1.4). Индол-3-лактат образуется из индол-3пирувата в результате реакции восстановления, которую катализирует ароматическая 2-оксокислотредуктаза (ЕС: 1.1.1.110), тогда как индол-3-пируват образуется благодаря трем ферментам: триптофантрансаминазе (ЕС: 2.6.1.27), L-триптофанпируватаминотрансферазе (ЕС: 2.6.1.99) и оксидазе-L-аминокислот (ЕС: 1.4.2.2). Дальнейшее превращение индол-3-лактата возможно в индол-3-акрилат ферментом 3-(арил)-акрилоилКоА(арил)лактат-КоА-трансферазой (ЕС: 2.8.3.17) [17]. Следует отметить, что метаболит, который образуется из индол-3-лактата (индол-3-акрилат), активирует фермент индолпируватдекарбоксилазу (ЕС: 4.1.1.74), который принимает участие в превращении индол-3-пирувата по индол-3-ацетатному пути [17] (рис. 1).
В работах, посвященных изучению ожирения, показано, что происходит повышение концентрации индол-3-ацетата, индол-3-лактата и индола в крови больных [8, 18]. В то же время многие авторы описывают таксономическое обеднение микробиоты у больных с ожирением [19, 20]. Доказана роль индол-3-ацетата и индол-3-пропионата в подавлении воспаления, которое способствует ремоделированию жировой ткани и развитию инсулинорезистентности [21]. Не вызывает сомнений, что коррекция диеты значимо меняет таксономический состав микробиоты в кишечнике. Однако насколько стойкими будут эти изменения и как быстро произойдет возврат к характерному для ожирения фенотипу дисбиоза, ответить пока сложно, и очень часто эти показатели будут носить индивидуальный характер для каждого конкретного больного [22].
Таким образом, остается открытым вопрос о составе продуцентов отдельных метаболитов триптофана, гомеостатической стабильности этого состава в норме и при ожирении, а также места этих метаболитов в общем метаболическом профиле микробного сообщества кишечника и их влияние на ферментативный ландшафт микробиома кишечника. Под «ферментативным ландшафтом» (представленностью генов ферментов) мы понимаем наличие и содержание (в условных единицах) генов различных ферментов, т. е. возможное ферментативное присутствие в соответствии с представленностью ДНК микроорганизмов, которые потенциально могут экспрессировать тот или иной фермент.
Целью нашего исследования было изучение содержания метаболитов обмена триптофана в экстрактах кала и их взаимосвязи с прогностической представленностью генов ферментов микробиома кишечника у больных ожирением.
ПАЦИЕНТЫ И МЕТОДЫ
Группа исследования
Обследовано 223 пациента, средний возраст которых составил 39,9 ± 4,2 года. Сформированы две клинические группы. Группа 1 (n = 109) — контрольная группа здоровых добровольцев, не имеющих ожирения и/или метаболического синдрома, со средним индексом массы тела (ИМТ) — 19,8 [18,5–22,0] кг/м2 и объемом талии (ОТ) — 73,0 [68,0–74,5] см. Критерии включения в группу 1: возраст от 30 до 50 лет, ИМТ < 25 кг/м2, ОТ < 80 см для женщин и < 94 см для мужчин; отсутствие приема антибиотиков, пребиотических и пробиотических препаратов в течение трех месяцев до включения в исследование подписанное информированное согласие на участие в исследовании. Критерии исключения из группы 1: беременность и грудное вскармливание, декомпенсация хронических заболеваний, наличие онкопатологии, наследственные патологии триптофанового обмена в анамнезе, острые респираторные вирусные инфекции; любые заболевания желудочно-кишечного тракта (в том числе неспецифический язвенный колит, болезнь Крона, синдром раздраженного кишечника); депрессия; алкоголизм и отсутствие ожирения и/или метаболического синдрома. Группа 2 (n = 114) — группа наблюдения с ожирением и/или метаболическим синдромом со средним ИМТ — 33,0 [31,0–36,0] кг/м2 и ОТ — 90,0 [96,0–105,0] см. Критерии включения в группу 2: возраст от 30 до 50 лет, ИМТ — 30–34,9 кг/м2, ОТ > 80 см для женщин и > 94 см для мужчин; отсутствие приема антибиотиков, пребиотических и пробиотических препаратов в течение трех месяцев до включения в исследование, подписанное информированное согласие на участие в исследовании. Критерии исключения из группы 2: беременность и грудное вскармливание, декомпенсация хронических заболеваний, наличие онкопатологии, наследственные патологии триптофанового обмена в анамнезе, острые респираторные вирусные инфекции; любые заболевания желудочно-кишечного тракта (в том числе неспецифический язвенный колит, болезнь Крона, синдром раздраженного кишечника); депрессия; алкоголизм. Пациенты групп наблюдения не придерживались какой-либо диеты. От каждого участника исследования был получен образец фекалий. С целью минимизации влияния климатических условий, характера питания и этнических факторов на кишечный микробиом в исследование были включены лица, проживающие на одной территории (Ростовская область и город Ростов-на-Дону) в осенне-летний период.
Хроматографический анализ
От всех участников исследования были получены образцы кала согласно протоколу исследования. Транспортировку и хранение образцов осуществляли с соблюдением холодовой цепи при температуре не выше –40 °С.
Количественный анализ метаболитов обмена триптофана в кале проводили методом высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием (ВЭЖХ-МС/МС). Анализ проводили при помощи жидкостного хроматографа Agilent 1290 (Agilent inc.; США) с системой автоматического ввода образцов, термостатом колонки и дегазатором. Для подготовки образцов кала его лиофилизировали до сухого остатка, далее навеску около 5 мг экстрагировали 50% метанолом в воде с добавлением внутреннего стандарта и аскорбиновой кислоты. После центрифугирования образец анализировали методом ВЭЖХ-МС/МС.
Хроматографическое разделение проводили с использованием аналитической колонки Discovery PFP HS F5 (2,1 × 150 мм; 3 мкм, Supelco Inc, St. Louis, Missouri,
USA). Для детектирования использовали массспектрометрический детектор на основе тройного квадруполя Agilent 6470 (Agilent inc.; США) MRM и электрораспылительной ионизацией. Характеристические для каждого соединения родительские и дочерние ионы для режима MRM, а также параметры ионизации и диссоциации оптимизировали с использованием стандартов исследуемых метаболитов. Полученный сигнал обрабатывали при помощи программного обеспечения Masshunter (Agilent inc.; США).
Температуру колонки и скорость потока устанавливали на 40 °С и 0,4 мл/мин соответственно. Подвижные фазы состоят из 0,1% водного раствора муравьиной кислоты (фаза А) и ацетонитрила (фаза В). Программа градиента была следующей: 0 мин — 1% В; 4 мин — 10% В; 9 мин — 90% В; 10 мин — 90% В; 10,1 — 1% В; 12 мин — 1% B. Ионизация электрораспылением работала в положительном режиме. Основные параметры МС были следующими: температура газа — 300 °С; расход газа — 8 л/мин; газ для распыления — 20 фунтов на квадратный дюйм; нагреватель защитного газа — 300; расход защитного газа — 10 л/мин; капиллярное напряжение — 3500 кВ.
Расчет концентраций метаболитов проводили методом внутреннего стандарта (2-гидроксиникотиновая кислота). Стандарты определяемых соединений готовили с использованием искусственной матрицы, содержащей бычий сывороточный альбумин и хлорид натрия. В матрицу добавляли исследуемые метаболиты и проводили подготовку согласно методике анализа.
Методика была валидирована по показателям селективности, линейности, точности, воспроизводимости, матричному эффекту и стабильности аналита. Валидацию проводили в соответствии с руководством по валидации биоаналитических методик FDA. Образцы кала лиофилизировали до сухого остатка, затем образец массой около 5 мг экстрагировали 50%-ным раствором метанола в воде с добавлением внутреннего стандарта и аскорбиновой кислоты. Пробоподготовку проводили следующим образом: 100 мкл каловых спиртовых экстрактов (калибраторы или КК) смешивали с раствором внутреннего стандарта 10 мкл исходного раствора, 10 мкг/мл раствора 2-гидроксиникотиновой кислоты и 400 мкл ацетонитрила. Затем смесь встряхивали, центрифугировали в течение 10 мин при 13 000 об./мин и выпаривали досуха в вакуумном центрифужном испарителе при 37 °С. Остатки далее восстанавливали 100 мкл раствора 0,02% аскорбиновой кислоты в 10%-м метаноле, центрифугировали и переносили в пробирку для ЖХ-МС. 5 мкл экстракта вводили в жидкостный хроматограф для последующего анализа методом ВЭЖХ– МС/МС.
Секвенирование (V3-V4 региона) гена 16S рРНК
Из образцов фекалий проводили выделение бактериальной ДНК с использованием наборов QIAamp Fast DNA Stool Mini Kit (QIAGEN GmbH; Германия). Полученную бактериальную ДНК амплифицировали с использованием праймеров, специфичных к вариабельному участку V3-V4 гена 16S рРНК. После очистки смеси парамагнитными частицами AMPure XP (Beckman Coulter; США) ПЦР-продукты индексировали с помощью индекс-праймеров Nextera XT Index Kit (Illumina, Inc.; США). Повторно выполняли очистку смеси парамагнитными частицами и сформированные библиотеки секвенировали на платформе MiSeq (Illumina, Inc.; США) согласно протоколу производителя.
Техническая обработка результатов секвенирования
Для полученных ридов был проведен контроль качества с помощью программы fastQC по следующим критериям: 1) распределение качества оснований — минимум 90% с качеством > 25; 2) распределение длины ридов — минимум 90% прочтений достигают длины в 300 нуклеотидов; 3) максимальный процент неопределенных оснований — 1.
Полученные последовательности генов были проанализированы с помощью программы «QIIME v.1.9.1» с использованием референсной базы данных «Greengenes v.13.8» с 97%-ным порогом сходства между последовательностями. Данные представленности бактериальных таксонов в общем пуле ридов были получены в долях (от 0 до 1), рассчитанных на основе количества картированных ридов для каждого таксона. Для характеристики альфа-разнообразия кишечного микробиома было рассчитано общее количество наблюдаемых операционных таксономических единиц (Observed OTUs). Операционная таксономическая единица — суррогатный таксономический уровень, результат кластерного объединения результатов секвенирования генов 16s РНК бактерий.
Биоинформационный анализ
Первичную обработку данных секвенирования и получение списка OTU осуществляли в программе «QIIME v.1.9.1» [23]. Вторым этапом проводили анализ предположительной метаболической роли участников микробиоты путем реконструкции ненаблюдаемых состояний при помощи PICRUSt [24].
Изучение прогностической представленности генов ферментов проводили с использованием биоинформационного анализа, в процессе которого было предусмотрено сопоставление данных метагеномного секвенирования с базой данных энциклопедии KEGG Enzymes, при помощи PICRUSt [24]. Результаты анализа прогностической представленности генов ферментов указаны в относительных единицах, и их можно сравнивать между образцами и когортами исследуемых групп в рамках одного проекта.
Статистический анализ результатов исследования проводили с использованием пакета программы STATISTICA 12.0 (StatSoft Inc; США). Все полученные массивы данных были проверены на нормальность распределения с использованием критерия Шапиро–Уилка. Распределение носило нормальный характер и данные были представлены в виде среднего и стандартного отклонения.
В таблицах приведен коэффициент корреляции Спирмена. Корреляционный анализ проведен с оценкой статистической значимости коэффициента корреляции. Статистически значимым различие принимали при p < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Содержание катаболитов триптофана в кале
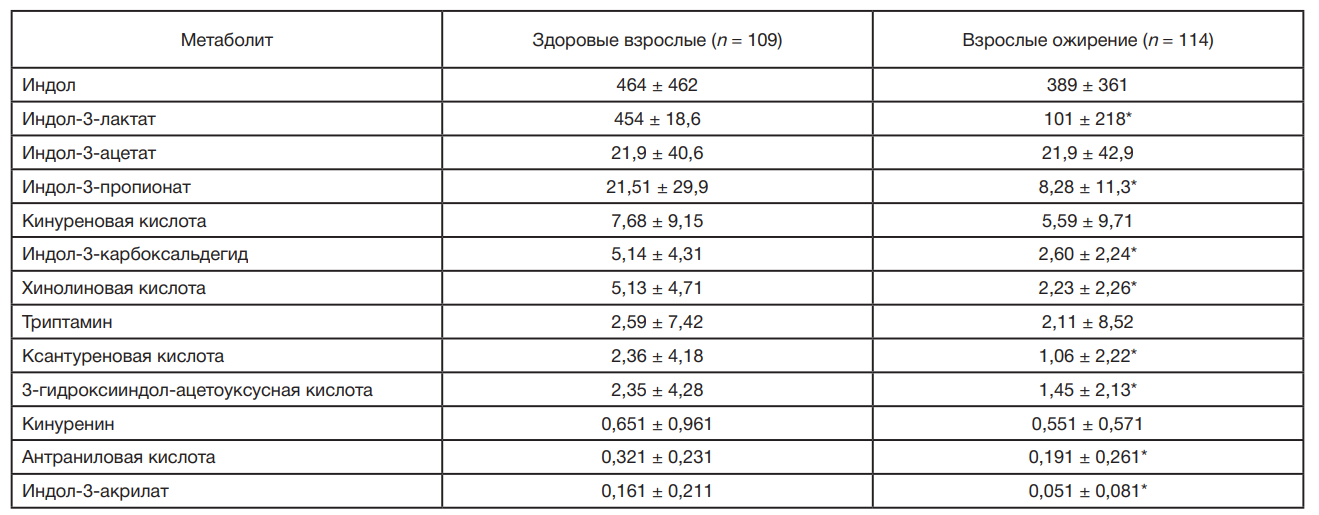
При анализе содержания триптофановых катаболитов в кале нами установлено, что доминантными MICT являются индол и индол-3-лактат (табл. 1).
В кале взрослых больных ожирением статистически значимо снижена концентрация восьми метаболитов обмена триптофана по сравнению со здоровыми донорами: индол-3-лактата, хинолиновой кислоты, 3-гидросииндолацетоуксусной кислоты, антраниловой кислоты, ксантуреновой кислоты, индол-3-карбоксальдегида, индол-3-акрилата и индол-3-пропионата. Следует отметить, что содержание индол-3-лактата в кале у больных с ожирением резко снижено, и среднее значение содержания данного метаболита триптофана на 78% снижено в сравнении с нормой (табл. 1).
Взаимосвязь содержания катаболитов триптофана в кале с прогностической представленностью генов ферментов кишечной микробиоты
С помощью PICRUSt-анализа таксономического разнообразия микробиома мы оценили количественную прогностическую представленность генов различных ферментов в соответствии с количественной представленностью ДНК тех или иных микроорганизмов кишечника в норме и при ожирении, а затем провели корреляционный анализ между прогностической ферментативной представленностью микробиоты кишечника и содержанием триптофановых катаболитов в кале.
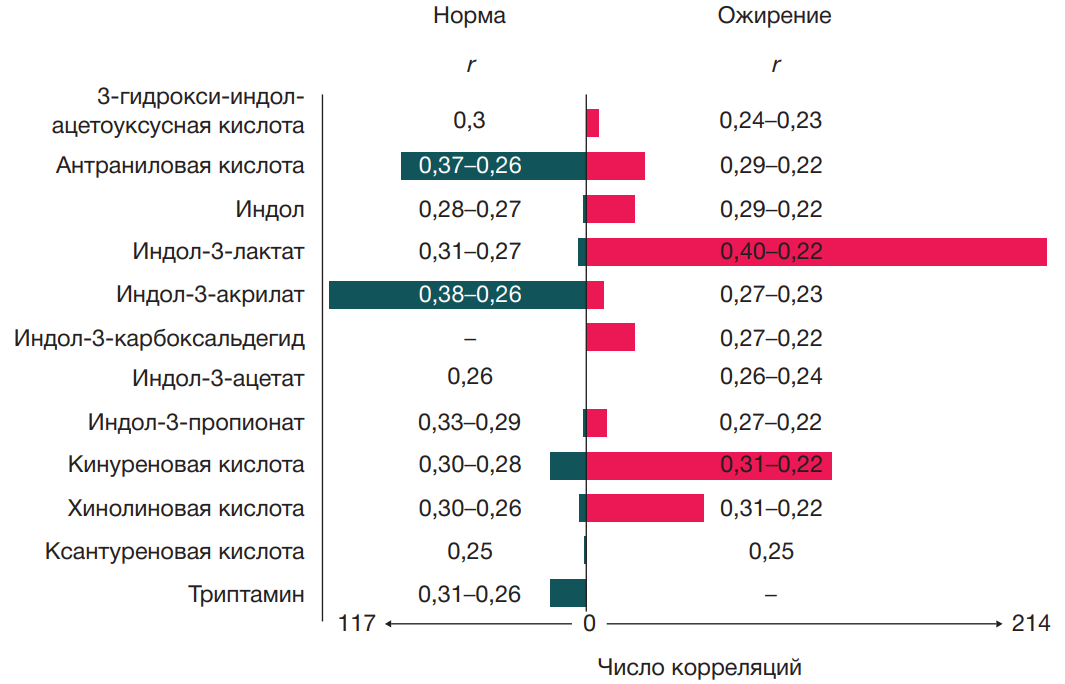
Установили, что у лиц с ожирением наблюдается более выраженное сопряжение между прогностической представленностью генов ферментов микробиоты кишечника и метаболитами обмена триптофана. Так, у здоровых обследуемых нами установлена 251 статистически значимая корреляционная связь (significance level = 3, р ≤ 0,001), тогда как у лиц с ожирением — 479 статистически значимых взаимосвязи с таким же уровнем достоверности (рис. 2).
Установили, что при ожирении содержание индола в кале статистически значимо не изменялось (табл. 1), тогда как прогностическая представленность генов ферментов микробиома кишечника, с которыми коррелирует содержание индола, увеличивалась в 10 раз (рис. 2).
Для второго доминантного катаболита обмена триптофана в кишечнике — индол-3-лактата мы установили статистически значимое снижение содержания в кале данного метаболита при ожирении (табл. 1). Однако при этом количество статистически значимых корреляционных пар для индол-3-лактата и прогностической представленности генов различных ферментов микробиома кишечника с пяти пар, установленных нами в норме, увеличивается до 214 пар у лиц с ожирением (рис. 2).
У больных с ожирением нами установлено, что потенциально ключевыми сигнальными метаболитами триптофана, коррелирующими с прогностической представленностью генов ферментов микробиома кишечника, являются: индол, индол-3-лактат, кинуреновая и хинолиновая кислоты. Тогда как у лиц без ожирения такими ключевыми сигнальными молекулами являются индол-3-акрилат и антраниловая кислота (рис. 2).
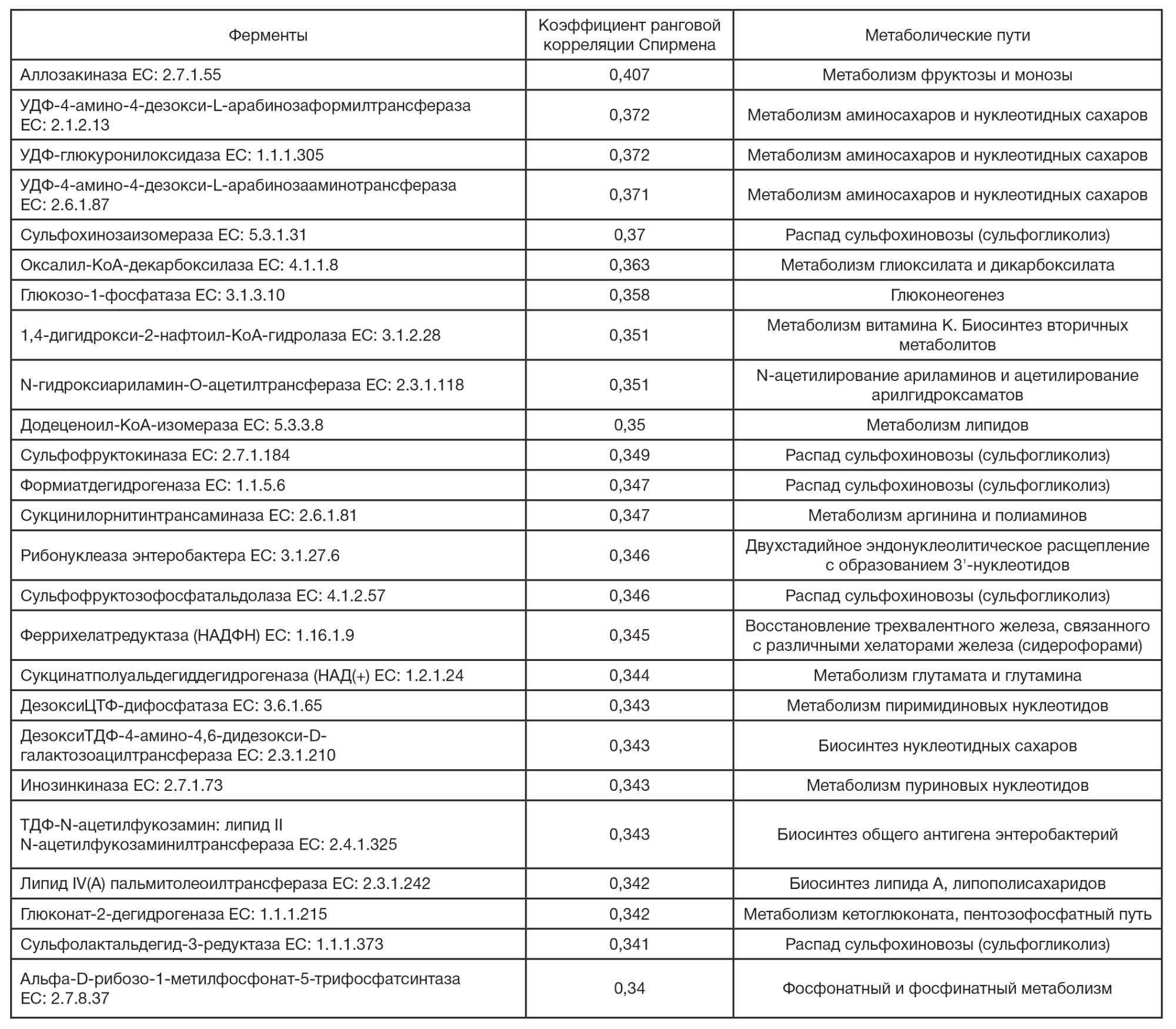
При дальнейшем анализе нами установлены ферменты, прогностическая представленность генов которых более тесно коррелирует (коэффициент ранговой корреляции Спирмена — 0,407-0,340) с содержанием в кале индол-3лактата (табл. 2).
Среди ферментов микробиома, прогностическая представленность генов которых коррелирует с содержанием индол-3-лактата в кишечнике у больных с ожирением, нами установлены ферменты обмена углеводов, аминокислот, полиаминов, нуклеотидов и сульфосахаров (табл. 2).
Установлено также, что содержание индол-3-лактата в кале коррелирует с прогностической представленностью генов ферментов метаболизма аминокислот: аргинина, глутамата и глутамина.
Взаимосвязь таксономической представленности микроорганизмов кишечника с содержанием индол-3-лактата в кале
Анализ представленности бактерий и архей на уровне семейств (Phylum – f), родов (Genus – g) и видов (Species – s) у здоровых обследуемых позволил установить, что с концентрацией индол-3-лактата в кале статистически значимо взаимосвязана представленность следующих семейств микроорганизмов: Ruminococcaceae, Lachnospiraceae, Akkermansiaceae, Barnesiellaceae (приложение 1).
В то же время мы установили, что у больных ожирением с индол-3-лактатом в кале статистически значимо взаимосвязаны другие представители микробиоты кишечника, такие как: Enterobacteriaceae и Pseudomonadaceae (приложение 2). Важно отметить, что при ожирении микроорганизмы, содержание которых коррелирует с содержанием индол-3-лактата в кишечнике, отличаются от нормы. Если в норме мы установили наличие 54 статистически значимых корреляционных связей между различными видами микроорганизмов в кишечнике и индол-3-лактатом, то у пациентов с ожирением статистически значимых корреляционных связей было в три раза больше (154 пары).
В результате проведенного нами анализа не установлено статистически значимых корреляционных связей между индол-3-лактатом и представленностью в кишечнике Klebsiella, Pseudomonas, Escherichia-Shigella для лиц с нормальной массой тела. Очевидно, что при ожирении индол-3-лактат в кишечнике продуцирует преимущественно семейство Enterobacteriaceae. Важно отметить, что, согласно литературным данным, ожирение приводит к таксономическому обеднению микробиома кишечника [19]. Однако в нашем исследовании установлено, что при ожирении происходит, напротив, обогащение представленности таксонов микробиоты кишечника, которая является потенциальным продуцентом индол-3-лактата.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Интересен тот факт, что у лиц с ожирением снижается содержание катаболитов обмена триптофана в кале, и максимальное снижение установлено именно для индол3-лактата. При этом именно данный метаболит является доминантным как в норме, так и при ожирении. Однако только при ожирении мы регистрируем ключевую роль индол-3-лактата в плане потенциального регулятора прогностической представленности генов ферментов микробиома кишечника. Нами установлено 214 различных фермента, прогностическая представленность которых потенциально зависит от индол-3-лактата.
Одной из важных мишеней для индол-3-лактата в патогенезе ожирения мы считаем установленные нами прогностические представленности для ферментов обмена полиаминов. Известно, что полиамины образуются микробиотой кишечника из аргинина и его продукта — орнитина [20]. Метаболизм полиаминов играет центральную роль в регуляции системного и мукозального адаптивного иммунитета. В свою очередь, аргинин — важный модулятор метаболизма макрофагов и Т-клеток, способный влиять на их эффекторные функции. Кроме того, полиамины ингибируют выработку провоспалительных цитокинов и обладают антиоксидантным эффектом [25]. В кишечнике полиамины могут снижать высвобождение цитокинов, что способствует лучшей репарации поврежденного эпителия и восстановлению нормальной барьерной функции. Спермин (полиамин) ингибирует активацию инфламмасомы, представляющей собой белковый комплекс, экспрессируемый эпителиальными клетками, который может регулировать секрецию ИЛ-18 [25]. Было также, показано, что присутствие пробиотического штамма Bifidobacterium animalis может индуцировать устойчивость к окислительному стрессу и способствовать увеличению продолжительности жизни, которая зависит от усиленного микробного синтеза полиаминов [26]. По литературным данным, повышенный уровень полиаминов в белой жировой ткани, печени или скелетных мышцах может стимулировать энергетический обмен и устойчивость к развитию алиментарного ожирения [27]. Также известно, что метаболиты полиаминов участвуют в адипогенезе [28]. Было показано, что лечение экзогенным спермином эффективно снижает массу тела и уровень глюкозы натощак, а также улучшает толерантность к глюкозе у мышей с ожирением, связанным с диетой [29]. Кроме того, спермин влияет на рецепцию инсулина и инсулиносенситивность [30]. Таким образом иммунологические и метаболические эффекты полиаминов во многом совпадают с эффектами сигнальной системы «индолы-AhR». Найденные нами корреляции могут свидетельствовать о совместном участии индол-3-лактата и полиаминов в механизмах толерогенности (или их нарушений) у больных с ожирением, а совместное снижение этих двух механизмов толерогенности при ожирении возможно приводит к повышенной проницаемости кишечника.
Взаимосвязь уровня индол-3-лактата в кале и прогностической представленности генов ферментов сульфогликолиза микробиома кишечника пока не совсем изучена. Сульфосахар сульфохиновоза (SQ) вырабатывается практически всеми фотосинтезирующими организмами на Земле и метаболизируется бактериями в процессе сульфогликолиза. Сульфогликолитический путь Эмбдена–Мейергофа–Парнаса метаболизирует SQ с образованием дигидроксиацетонфосфата и сульфолактатальдегида и аналогичен классическому пути гликолиза [31, 32]. В литературе есть работы, которые идентифицируют микроорганизмы, принимающие участие в сульфогликолизе [33]. Однако нет исследований, оценивающих взаимосвязь метаболитов сульфогликолиза с содержанием индольных метаболитов триптофанового обмена. Мы установили наличие статистически значимых взаимосвязей между прогностической представленностью генов ферментов сульфогликолиза микробиома кишечника и концентрацией индол-3-лактата в кале у лиц с ожирением (рис. 3). Следует отметить, что сульфосахара являются резервуарами сульфата, который потенциально может быть использован для синтеза гликозаминогликанов и ремоделирования внеклеточного матрикса, что имеет важное значение как для развития хронического вялотекущего воспаления при ожирении, так и для формирования протуморогенного фенотипа, что характерно для лиц с ожирением [21].
Важно отметить, что нами не было установлено статистически значимых взаимосвязей между содержанием катаболитов триптофана в кале и прогностической представленностью генов ферментов микробиома кишечника, которые принимают участие в их продукции.
При ожирении происходит изменение генотипа и возможно фенотипа микробиоты кишечника: в три раза увеличивается количество таксонов, которые потенциально могут быть поставщиками индол-3-лактата. При этом значимое снижение концентрации индол-3лактата в кале может отражать выраженное бактериальное обсеменение кишечника и повышенное потребление данного триптофанового катаболита соответствующими таксонами микробиоты, которые характерны для больных с ожирением. Именно для содержания индол-3-лактата в кале количественно увеличиваются статистически значимые взаимосвязи с прогностической представленностью генов ферментов углеводного, липидного, нуклеотидного и аминокислотного обменов, а также сульфогликолиза. На популяционном уровне микробиота, в том числе кишечника, считается стабильной и эволюционно отобранной. При этом комменсальную микробиоту можно качественно и количественно модулировать [19] диетой, различными сигнальными молекулами и цитокинами. Возможно, что обогащение таксонов, продуцирующих индол-3-лактат, происходит компенсаторно с целью подавления продукции провоспалительных цитокинов, которая, как правило, сопровождает пациентов с ожирением. Так, известно, что индол-3-лактат оказывает выраженное противовоспалительное действие — участвует в индукции иммуннорегуляторных Т-клеток и подавлении воспалительных Т-клеток [34]. Из недавних исследований известно, что индол-3-лактат является доминантным катаболитом триптофана для Bifidobacterium (B. longum subsp. infantis). Кроме того, достаточно высокий уровень индол-3-лактата содержится в грудном молоке женщин [34]. Нами же показано, что содержание индол3-лактата в кале у пациентов с ожирением потенциально зависит от таксономической представленности семейства Enterobacteriaceae. Снижение данного семейства микробиоты кишечника коррелирует со снижением индол3-лактата у лиц с ожирением. Однако, если учитывать установленное нами ранее повышение индол-3-лактата в сыворотке крови лиц с ожирением [18], вполне вероятно, что образование данного MICT в кишечнике стабильное или даже повышенное, тогда как транспорт из кишечника в кровь индол-3-лактата у больных с ожирением может быть интенсифицирован. Ответ еще предстоит найти, так как источником индол-3-лактата может быть не только микробиота кишечника, но и микробиота других экологических ниш организма человека.
ВЫВОДЫ
Доминантными катаболитами триптофана являются индол и индол-3-лактат как у здоровых лиц, так и у лиц с ожирением. В кале у пациентов с ожирением статистически значимо снижена концентрация: индол-3-лактата, хинолиновой кислоты, 3-гидросииндолацетоуксусной кислоты, антраниловой кислоты, ксантуреновой кислоты, индол-3-карбоксальдегида, индол-3-акрилата и индол-3пропионата. Максимальное снижение отмечено именно для индол-3-лактата. У лиц с ожирением отмечается более выраженное сопряжение между прогностической представленностью генов ферментов микробиома кишечника и MICT. В группе здоровых обследуемых представленность генов ферментов микробиома кишечника коррелирует с содержанием индол-3-акрилата и антраниловой кислоты. Тогда как для лиц с ожирением другие MICT (индол и индол3-лактат), а также хинолиновая и кинуреновая кислоты, определяют «ферментативный ландшафт» микробиома кишечника. Более тесные корреляционные связи между прогностической представленностью генов ферментов микробиома кишечника и MICT были установлены именно для индол-3-лактата. Установлено, что содержание индол-3-лактата в кале коррелирует с прогностической представленностью генов ферментов микробиома кишечника, включающих метаболизм углеводов, нуклеотидов, аминокислот, полиаминов и сульфосахаров. Не установлено статистически значимых корреляционных связей между содержанием катаболитов триптофана и прогностической представленностью генов ферментов, которые принимают участие в их образовании. У пациентов с ожирением исследуемой популяции установлено увеличение разнообразия таксонов потенциальных продуцентов индол-3-лактата. Потенциальная коррекция метаболичеcкой активности микробиоты кишечника катаболитами триптофана может иметь профилактическое и терапевтическое значение для больных ожирением.
- Bharti К, Grimm DJ. Current challenges and best-practice protocols for microbiome analysis Briefings. in Bioinformatics. 2021; 22 (1): 178–93. PubMed PMID: 31848574.
- Singer-Englar T, Barlow G, Mathur R. Obesity, diabetes, and the gut microbiome: an updated review. Expert Rev Gastroenterol Hepatol. 2019; 13 (1): 3–15. PubMed PMID: 30791839.
- Franzosa EA, Sirota-Madi A, Avila-Pacheco J, Fornelos N, Haiser HJ, Reinker S, et al. Gut microbiome structure and metabolic activity in inflammatory bowel disease. Nat Microbiol. 2019; 4 (2): 293– 305. PubMed PMID: 30531976.
- Halfvarson J, Brislawn CJ, Lamendella R, Vázquez-Baeza Y, Walters WA, Bramer LM, et al. Dynamics of the human gut microbiome in inflammatory bowel disease. Nat Microbiol. 2017; 13 (2): 17004. PubMed PMID: 28741610.
- Kiyohara H, Sujino T, Teratani T, Miyamoto K, Arai MM, Nomura E, et al. Toll-like receptor 7 agonist-induced dermatitis causes severe dextran sulfate sodium colitis by altering the gut microbiome and immune cells. Cell Mol Gastroenterol Hepatol. 2018; 25 (7): 135– 56. PubMed PMID: 30510995.
- Desai SN, Landay AL. HIV and aging: role of the microbiome. Curr Opin HIV AIDS. 2018; 13 (1): 22–27. PubMed PMID: 29035948.
- Burcelin R. HIV and aging: role of the microbiome. Biol Aujourdhui. 2017; 211 (1): 1-18. PubMed PMID: 28682223. French.
- Roager HM, Licht TR. Microbial tryptophan catabolites in health and disease. Nat Commun. 2018; 9 (1): 3294. PubMed PMID: 30120222.
- Scott SA, Fu J, Chang PV. Microbial tryptophan metabolites regulate gut barrier function via the aryl hydrocarbon receptor. Proc Natl Acad Sci USA. 2020; 117 (32): 19376–87. PubMed PMID: 32719140.
- Wong CB, Tanaka A, Kuhara T, Xiao JZ. Microbial tryptophan metabolites regulate gut barrier function via the aryl hydrocarbon receptor. Microorganisms. 2020; 8 (3): 398. PubMed PMID: 32178456.
- Aust AC, Benesova E, Vidova V, Coufalikova K, Smetanova S, Borek I, et al. Profiling tryptophan catabolites of human gut microbiota and acute-phase protein levels in neonatal dried blood specimens. Front Microbiol. 2021; 12: 665743. PubMed PMID: 34777268.
- Thursby E, Juge N. Introduction to the human gut microbiota. Biochem J. 2017; 474: 1823–36. PubMed PMID: 34777268.
- Vyhlídalová B, Krasulová K, Pečinková P, Vyhlídalová B, Krasulová K, Pečinková P, et al. Gut microbial catabolites of tryptophan are ligands and agonists of the aryl hydrocarbon receptor: a detailed characterization. Int J Mol Sci. 2020; 21 (7): 2614. PubMed PMID: 32283770.
- Yoval-Sánchez B, Pardo JP, Rodríguez-Zavala JS. New insights into the half-of-the-sites reactivity of human aldehyde dehydrogenase 1A1. Proteins. 2013; 81 (8): 1330–9. DOI: 10.1002/prot.24274.
- Qu Y, Dai C, Zhang X, Ma Q. A new interspecies and interkingdom signaling molecule-Indole. Sheng Wu Gong Cheng Xue Bao. 2019; 35 (11): 2177–88. PubMed PMID: 31814363. Chinese.
- Ji Y, Gao Y, Chen H, Yin Y, Zhang W. Indole-3-acetic acid alleviates nonalcoholic fatty liver disease in mice via attenuation of hepatic lipogenesis, and oxidative and inflammatory stress. Nutrients. 2019; 11 (9): 2062. PubMed PMID: 31484323.
- Available from: https://www.genome.jp/pathway/map00380+C00954
- Shestopalov AV, Shatova OP, Karbyshev MS, Gaponov AM, Moskaleva NE, Appolonova SA, et al. «Kynurenine switch» and obesity. Bulletin of Siberian Medicine. 2021; 20: 103–11. DOI: 10.20538/1682-0363-2021-4-103-111].
- Mosca A, Leclerc M, Hugot JP. Gut microbiota diversity and human diseases: should we reintroduce key predators in our ecosystem? Front Microbiol. 2016; 7: 455. PubMed PMID: 27065999.
- Ramos-Molina B, Queipo-Ortuño MI, Lambertos A, Tinahones FJ, Peñafiel R. Dietary and gut microbiota polyamines in obesity- and age-related diseases. Front Nutr. 2019; 6: 24. PubMed PMID: 30923709.
- Silveira EA, da Silva Filho RR, Spexoto MC, Haghighatdoost F, Sarrafzadegan N, de Oliveira C. The role of sarcopenic obesity in cancer and cardiovascular disease: a synthesis of the evidence on pathophysiological aspects and clinical implications. Int J Mol Sci. 2012; 22 (9): 4339. PubMed PMID: 33919368.
- Zhang C, Yin A, Li H, Wang R, Wu G, Shen J, et al. Dietary modulation of gut microbiota contributes to alleviation of both genetic and simple obesity in children. EBioMedicine. 2015; 2 (8): 968–84. PubMed PMID: 26425705.
- Available from: http://qiime.org/
- Available from: https://picrust.github.io/picrust/
- Levy M, Thaiss CA, Elinav E. Metabolites: messengers between the microbiota and the immune system. Genes Dev. 2016; 30 (14): 1589–97. PubMed PMID: 27474437.
- Matsumoto M, Kurihara S, Kibe R, Ashida H, Benno Y. Longevity in mice is promoted by probiotic-induced suppression of colonic senescence dependent on upregulation of gut bacterial polyamine production. PLoS One. 2011; 6 (8): e23652. PubMed PMID: 21858192.
- Bonhoure N, Byrnes A, Moir RD, Hodroj W, Preitner F, Praz V, et al. Loss of the RNA polymerase III repressor MAF1 confers obesity resistance. Genes Dev. 2015; 29 (9): 934–47. PubMed PMID: 25934505.
- Ishii I, Ikeguchi Y, Mano H, Wada M, Pegg AE, Shirahata A. Polyamine metabolism is involved in adipogenesis of 3T3-L1 cells. Amino Acids. 2012; 42 (2-3): 619–26. PubMed PMID: 21809076.
- Sadasivan SK, Vasamsetti B, Singh J, Marikunte VV, Oommen AM, Jagannath MR, et al. Exogenous administration of spermine improves glucose utilization and decreases bodyweight in mice. Eur J Pharmacol. 2014; 729: 94–99. PubMed PMID: 24530553.
- Pedersen SB, Hougaard DM, Richelsen B. Polyamines in rat adipocytes: their localization and their effects on the insulin receptor binding. Mol Cell Endocrinol. 1989; 62 (2): 1661–6. PubMed PMID: 2663568.
- Sharma M, Abayakoon P, Epa R, Jin Y, Lingford JP, Shimada T, et al. Molecular basis of sulfosugar selectivity in sulfoglycolysis. ACS Cent Sci. 2021; 7 (3): 476–87. PubMed PMID: 33791429.
- Frommeyer B, Fiedler AW, Oehler SR, Hanson B, Loy A, Franchini P, et al. Environmental and intestinal phylum firmicutes bacteria metabolize the plant sugar sulfoquinovose via a 6-deoxy-6sulfofructose transaldolase pathway. iScience. 2020; 23 (9): 101510. PubMed PMID: 32919372.
- Haange SB, Groeger N, Froment J. Multiplexed quantitative assessment of the fate of taurine and sulfoquinovose in the intestinal microbiome. Metabolites. 2020; 10 (11): 430. PubMed PMID: 33114761.
- Huang W, Cho KY, Meng D, Walker WA. The impact of indole3-lactic acid on immature intestinal innate immunity and development: a transcriptomic analysis. Sci Rep. 2021; 11 (1): 8088. PubMed PMID: 33850185.