ОРИГИНАЛЬНОЕ ИССЛЕДОВАНИЕ
Зависимость иммуногенности и реактогенности кандидатной мРНК вакцины против туберкулеза от пола животных и дозы препарата
1 Автономная некоммерческая образовательная организация высшего образования «Научно-технологический университет «Сириус», Сириус, Россия
2 Центральный научно-исследовательский институт туберкулеза, Москва, Россия
3 Национальный исследовательский центр «Курчатовский институт», Москва, Россия
мРНК-вакцины показали высокую эффективность в борьбе с пандемией COVID-19 и другими вирусными инфекциями. Несмотря на интенсивное изучение мРНК-вакцин в последние пять лет, вопрос о безопасности их применения все еще остается актуальным. Целью работы было оценить иммуногенность противотуберкулезной мРНК вакцины в двух дозах у самок и самцов крыс через 2 и 4 недели после вакцинации. В эти же сроки определяли гематологические и биохимические показатели крови. Подтверждена дозозависимость иммуногенности мРНК вакцин как у самок, так и у самцов. Вакцинация привела к умеренной лимфоцитопении и нейтрофилии у самцов крыс, а также к выраженным дозо- и гендерзависимым изменениям в биохимических параметрах крови в различных временных точках. Полученные результаты свидетельствуют об умеренной токсичности противотуберкулезной мРНК вакцины и важности исследования ее токсических действий в различных временных точках у животных обоих полов.
Ключевые слова: туберкулез, токсичность, мРНК-вакцина, иммуногенность
Финансирование: исследование выполнено при поддержке Министерства науки и высшего образования Российской Федерации (соглашение № 075-10-2021-113, уникальный идентификатор проекта РФ----193021X0001).
Благодарности: авторы выражают благодарность сотрудникам АНО ВО «Университет «Сириус» И. М. Теренину за постановку транскрипции in vitro, О. В. Заборовой — за формуляцию мРНК в липидные наночастицы.
Вклад авторов: В. В. Решетников — подготовка мРНК вакцины, планирование эксперимента, написание рукописи; Г. С. Шепелькова — постановка экспериментов, анализ результатов; А. В. Рыбакова — постановка экспериментов, анализ результатов; А. П. Трашков — планирование эксперимента, редактирование рукописи; В. В. Еремеев — планирование эксперимента, редактирование рукописи; Р. А. Иванов — планирование эксперимента, редактирование рукописи.
Соблюдение этических стандартов: исследование одобрено этическим комитетом НИЦ «Курчатовский институт» (протокол № 2 от 31 октября 2023 г.), проведено в соответствии с Приказом Минздрава № 755 и Руководством Управления по охране лабораторных животных А5502-01.
Для корреспонденции: Василий Владимирович Решетников
Олимпийский пр-т, д. 1, г. Сочи, 354340, Россия; ur.hepsuitnalat@vv.vokintehser
В настоящее время активно ведется разработка новых мРНК-вакцин против различных вирусных и бактериальных инфекций, в том числе туберкулеза, для которых ранее разработанные живые, аттенуированные, рекомбинантные и ДНК-вакцины не показали приемлемой эффективности [1, 2]. Тем не менее существует много пробелов в нашем понимании биологии мРНК-вакцин, доставляемых с помощью липидных наночастиц (ЛНЧ). Известно, что мРНКЛНЧ имеют широкое биораспределение, обнаруживаются в большинстве тканей [3, 4], приводят к воспалительному ответу в месте введения и могут быть ассоциированы с нейровоспалением [5]. Накопилось немало свидетельств того, что применение вакцин на основе мРНК в некоторых случаях ассоциировано с развитием аллергических реакций, миокардитов и легочных кровотечений [6]. Вакцинирование мРНК-ЛНЧ в некоторых случаях приводит к отложенным во времени транскриптомным изменениям и умеренным изменениям уровня метилирования CpGостровков в периферических моноцитах крови [7]. Кроме того, сведений о биораспределении, а также времени элиминации мРНК вакцин и кодируемых ими антигенов недостаточно [4].
В доклинических испытаниях мРНК вакцин RNA-1273 и BNT162b2 против COVID-19 на крысах в первые сутки после вакцинации были показаны умеренное снижение массы и повышение температуры тела животных. Были выявлены также провоспалительные гематологические и биохимические изменения, повышение уровня цитокинов [8, 9]. Макроскопические изменения включали увеличение массы селезенки, печени и надпочечников, микроскопические —умеренное воспаление в месте инъекции, в паховой области, в подвздошных и подколенных лимфатических узлах, а также признаки воспаления в печени и селезенке. Все изменения носили дозозависимый характер, большинство показателей вернулось в состояние нормы через 2–3 недели после введения последней дозы препарата [8, 9]. Клинические исследования мРНК-вакцин RNA-1273, BNT162b2 и CS-2034 [10–12] тоже показали дозозависимые, местнораздражающие и системные нежелательные эффекты у некоторых участников, которые включали в себя воспаление в месте введения, усталость, головную боль, озноб, мышечную боль и боль в суставах, гематологические и биохимические изменения параметров крови. Нежелательные эффекты мРНК препаратов могут быть связаны как с действующим веществом вакцины — молекулой мРНК, так и с кодируемыми ею антигенами или липидными наночастицами, в которых инкапсулирована РНК.
Ранее мы показали, что разработанная нами противотуберкулезная мРНК-вакцина приводит к формированию адаптивного и протективного иммунного ответа [13]. Однако безопасность ее использования оставалась невыясненной. Цель данной работы — оценить токсическое действие двукратного введения противотуберкулезной мРНК-вакцины по изменению гематологических и биохимических параметров крови у самцов и самок крыс через 2 и 4 недели после вакцинации.
МАТЕРИАЛЫ И МЕТОДЫ
Животные
В эксперименте использовали 30 самок (126–149 г) и 30 самцов (154–180 г) крыс Wistar SPF-статуса возрастом 8–12 недель. Исследования проводили на базе питомника НИЦ Курчатовский институт, животных содержали в SPF-условиях при фиксированном световом режиме 12.00 : 12.00 ч и доступом к корму и воде ad libitum.
Дизайн эксперимента
Для работы было сформировано три экспериментальные группы, в каждой из них по 10 самцов и 10 самок:
группа I: группа с введением мРНК вакцины MTB-mEp5-1 в дозе 5 мкг/животное;
группа II: группа с введением мРНК вакцины MTB-mEp5-1 в дозе 15 мкг/животное;
группа III: группа с введением фосфатного буфера (PBS).
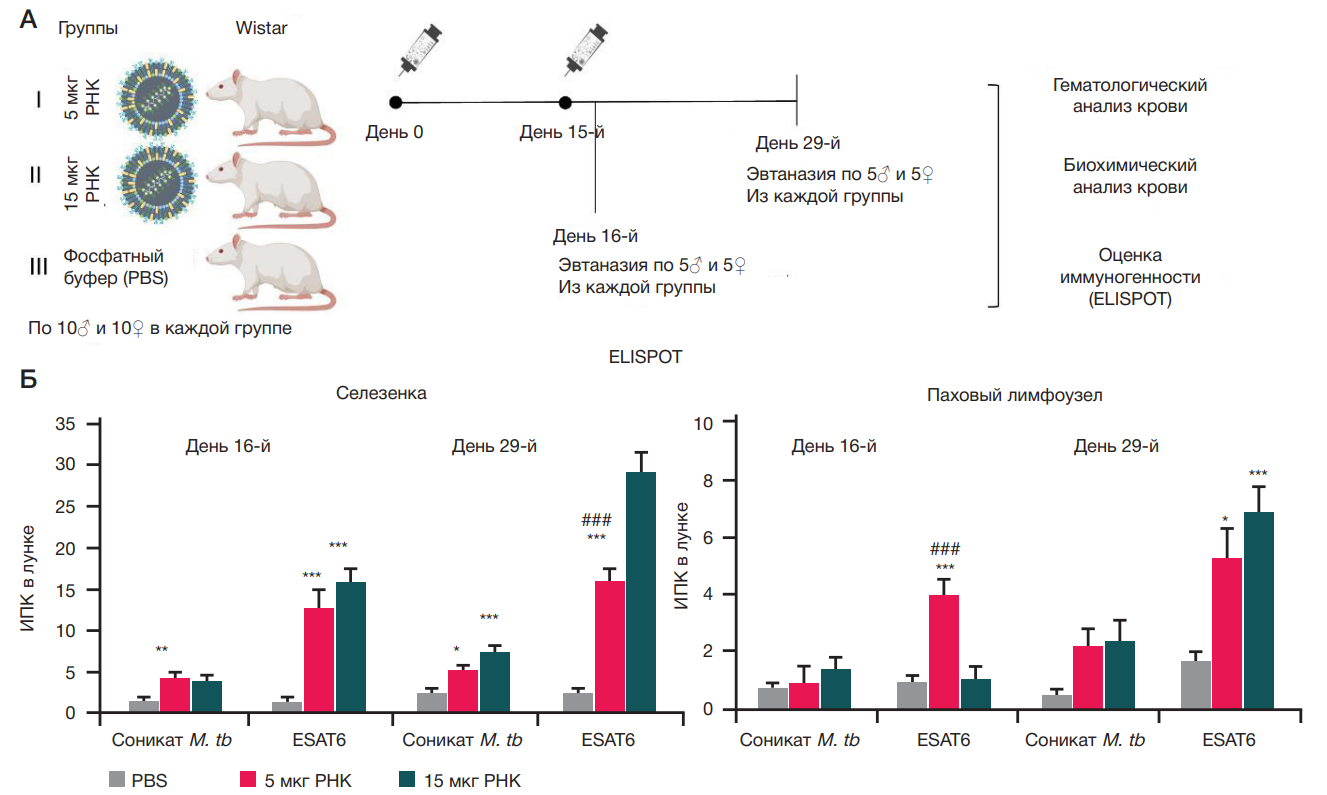
мРНК-вакцину или фосфатный буфер вводили экспериментальным животным двукратно с интервалом в 14 дней внутримышечно в область бедра с помощью трехкомпонентного инсулинового шприца с диаметром иглы 26 G в объеме 200 мкл (рисунокА). Животные были подвергнуты эвтаназии наркотизацией тилетамином/ золазепамом и ксилазином в дозах 15 мг/кг и 6 мг/кг, соответственно, с последующим обескровливанием полостей сердца и забором селезенки и паховых лимфоузлов. По пять самцов и пять самок из каждой группы были умерщвлены на 16-й день эксперимента (через 24 ч после повторного введения препарата), остальные животные — на 29-й день (через две недели после повторного введения препарата). У всех животных после умерщвления из полостей сердца была забрана кровь для клинического и биохимического анализа. Кроме того, для оценки иммуногенности мРНК вакцин были забраны паховые лимфоузлы и селезенка.
Используемые дозы мРНК вакцин соотносятся с дозой мРНК вакцины CVnCoV против COVID-19, которая в настоящее время проходит клинические испытания [NCT04652102]. MTB-mEp5-1 — вакцина с немодифицированным нуклеотидным составом (без использования аналогов уридина). Доза мРНК вакцины CVnCoV соответствует 12 мкг. Выбранные нами дозы исследуемой кандидатной вакцины — 5 и 15 мкг — являются близкими к дозам, используемым в клиническом исследовании, но без поправки на вес животного.
Вакцина MTB-mEp5-1
Мультиэпитопная мРНК вакцина MTB-mEp5-1 соответствует вакцине 5′-TPL-mEpitope-mRNA1273-3′, описанной ранее с незначительными модификациями [13]. В процессе in vitro транскрипции в качестве аналога кэпа был использован m7G(3'OMe)pppA(2'OMe)pG («Биолабмикс»; Россия) в концентрации 2,4 мм. Для специфической встройки этого аналога кэпа в процессе котранскрипционного кэпирования после последовательности T7 промотора в последовательность ДНК плазмиды был добавлен один аденин. Последовательность мРНК MTB-mEp5-1 представлена в Приложении 1.
Остальные описанные ранее [13] этапы наработки мРНК вакцинного препарата оставались без изменения. Формуляцию мРНК в липидные наночастицы осуществляли с помощью микрофлюидного картриджа на приборе NanoAssemblr™ Benchtop (Precision NanoSystems Inc; Канада). Частицы были сконцентрированы и стерилизованы с помощью PES-мембраны с диаметром пор 0,22 мкм. До момента введения препарата липидные наночастицы хранили при +4 °С не более 3 недель.
Аналитическую характеризацию полученных частиц проводили, как описано ранее [13], она включала оценку их размера, индекса полидисперсности, дзета-потенциала, процента загрузки мРНК в частицы и ее целостности. Размер частиц во всех экспериментальных группах был в диапазоне 86–88 нм, дзета-потенциал — в диапазоне от –3 до –2 мВ, индекс полидисперсности не превышал 0,1. Уровень загрузки РНК был более 90%, целостность РНК согласно данным капиллярного электрофореза — более 85%.
Гематологический и биохимический анализ крови
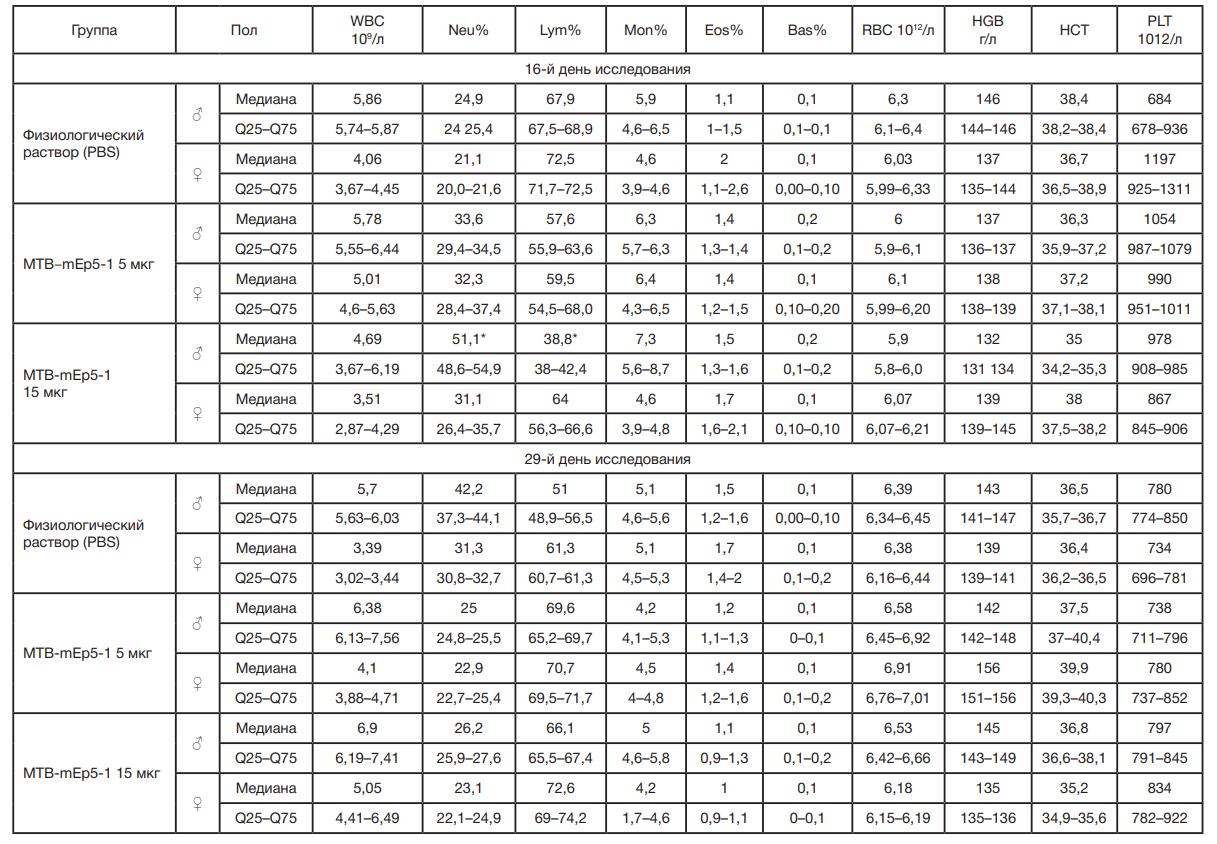
Для гематологических исследований кровь была собрана из полостей сердца в пробирки с антикоагулянтом (К3-ЭДТА), исследование проводили на гематологическом анализаторе DIATRON Abacus Junior 22.5. В образцах цельной крови определяли количество эритроцитов, уровень гемоглобина, гематокрит, количество лейкоцитов, количество тромбоцитов и лейкоцитарную формулу.
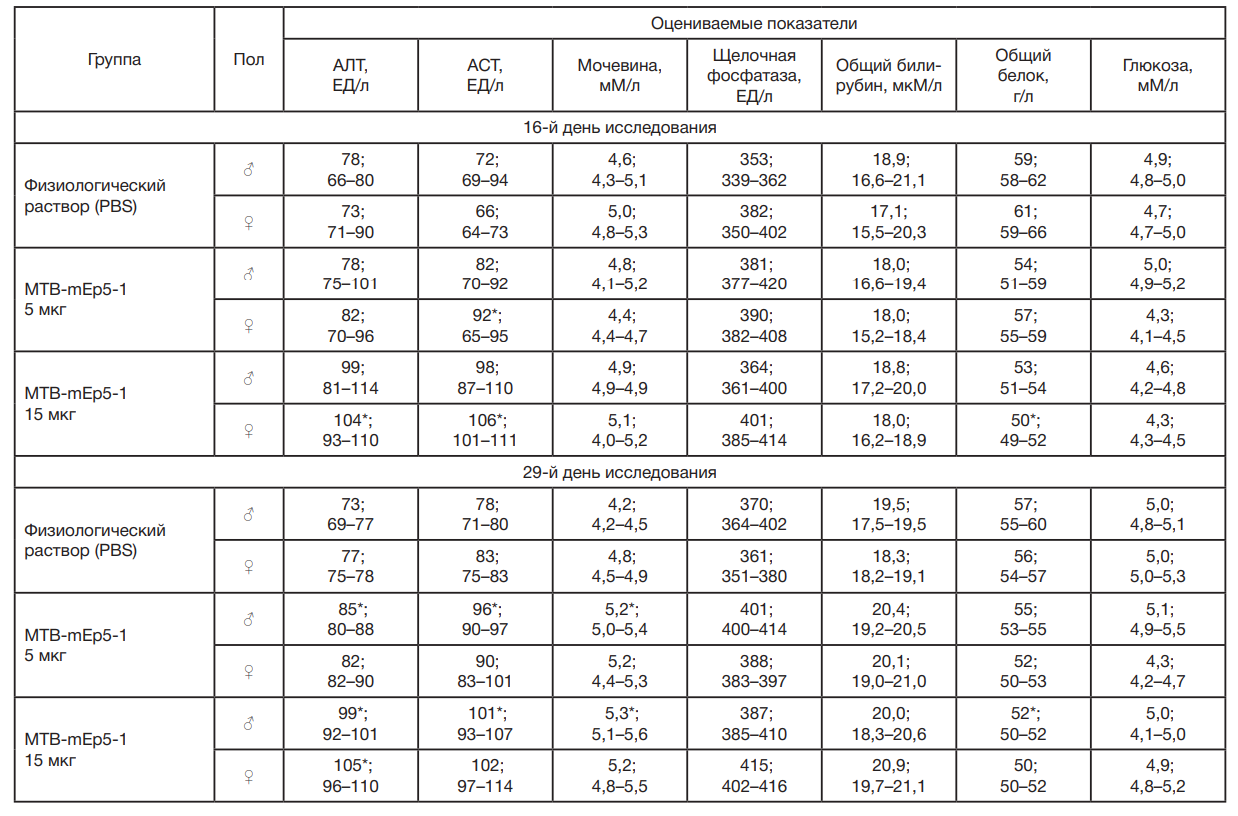
Для биохимического анализа крови образцы были забраны в пробирки с разделительным гелем, центрифугированы для получения сыворотки при 3000 g. В сыворотке была определена концентрация аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), мочевины, щелочной фосфатазы, общего билирубина, общего белка, глюкозы на биохимическом анализаторе Architect c8000 (Abbott, США).
Определение количества IFNγ-продуцирующих клеток
Уровень протективного Т-клеточного иммунного ответа оценивали по количеству выделенных из селезенки и паховых лифоузлов клеток, секретирующих IFNγ в ответ на стимуляцию микобактериальными антигенами (соникат M. tuberculosis) (10 мкг/мл) или рекомбинантным белком ESAT6 в концентрации 10 мкг/мл (методика получения ESAT6 описана ранее [14]) методом ELISPOT при помощи наборов Mouse IFNγ ELISpot Set (BD; США) и AEC Substrate Set (BD; США) в соответствии с рекомендациями изготовителей.
Статистический анализ данных
Все данные были проверены на нормальность распределения с помощью критерия Шапиро–Уилка (Shapiro‒Wilk`s W test). Были рассчитаны медиана и квартильный размах (Q25–Q75); межгрупповые сравнения (post hoc analysis) проведены с использованием критерия Тьюки (Tukey`s test analysis). Для комплексной оценки данных независимых групп в контрольных точках исследования был использован однофакторный дисперсионный анализ (ANOVA). Статистическую значимость определяли при р < 0,05. Статистический анализ был выполнен с помощью программного обеспечения Statistica 6.0 (StatSoft; США).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Оценка иммуногенности
Мы оценили влияние дозы вакцины на формирование адаптивного иммунного ответа у самок и самцов крыс в двух временных точках. Обнаружено значимое влияние иммунизации на уровень IFNγ-продуцирующих клеток (ИПК) после специфической стимуляции как в селезенке, так и в паховом лимфоузле (рисунокБ). Однако количество ИПК в селезенке было значительно выше. Мы также наблюдали выраженные различия в уровне ИПК на лунку в зависимости от типа специфической стимуляции (белок ESAT6 или соникат M. tb) как для клеток лимфоузла, так и для клеток селезенки в обеих временных точках. По всей вероятности, эти эффекты объясняются различной концентрацией целевого антигена в препарате, используемом для специфической стимуляции.
Оценка динамики формирования адаптивного иммунного ответа показала, что более выраженный ответ происходит на 29-й день эксперимента, через две недели после второй вакцинации, что хорошо согласуется с литературными данными.
Дозозависимые эффекты наблюдались после стимуляции ESAT6: на 16-й день эксперимента в клетках лимфоузлов уровень ИПК в группе I с введением дозы 5 мкг был выше, чем в группе II, и на 29-й день эксперимента в клетках селезенки уровень ИПК был почти в 2 раза выше у группы II по сравнению с группой I. Значимых различий в степени выраженности адаптивного иммунного ответа между самцами и самками не наблюдалось (p > 0,05).
Таким образом, наши результаты свидетельствуют о том, что двукратное внутримышечное введение мРНКвакцины MTB-mEp5-1 крысам приводит к формированию адаптивного иммунного ответа, который детектируется в двух исследуемых временных точках, и степень его выраженности зависит от дозы, но не от пола животного.
Оценка гематологических и биохимических изменений в крови
Мы не обнаружили существенного влияния вакцинации на показатели изучаемых параметров крови экспериментальных животных. Значимых изменений у самок всех экспериментальных групп в двух временных точках не наблюдалось (табл. 1). Лишь у самцов, иммунизированных вакциной MTB-mEp5-1 в дозе 15 мкг, на 16-е сутки исследования отмечалось значимое снижение медианных значений абсолютного (1,97 × 109/л против 3,78 × 109/л в группе PBS) и относительного уровня лимфоцитов (лимфоцитопения) и повышение медианных значений абсолютного (2,64 × 109/л против 0,89 × 109/л в группе PBS) и относительного уровня нейтрофилов (нейтрофилия). Однако эти параметры пришли в норму через две недели после второго введения вакцины, на 29-й день эксперимента.
При анализе основных биохимических показателей крови у получавших тестируемый препарат экспериментальных животных на 16-е и 29-е сутки исследования отмечались существенные изменения показателей результатов биохимического анализа. У самок крыс на 16-й день эксперимента вакцинация оказала влияние на уровень АЛТ, АСТ и общий белок в крови (ANOVA: F(2,12) = 4,03, p = 0,046; F(2,12) = 8,58, p = 0,005; F(2,12) = 9,05, p = 0,004 соответственно). Самки, иммунизированные MTB-mEp5-1 в дозе 15 мкг, демонстрировали повышение уровня АЛТ и АСТ и снижение уровня общего белка в крови. Самки, иммунизированные MTB-mEp5-1 в дозе 5 мкг, демонстрировали только повышение уровня АСТ. В то же время у самцов подобных изменений в биохимических показателях крови обнаружено не было.
На 29-й день эксперимента, изменения большинства биохимических параметров у самок крыс экспериментальных групп было нивелировано, за исключением АЛТ [ANOVA: F(2,12) = 14,12, p = 0,001], который оставался повышенным в группе MTB-mEp5-1 15 мкг. Напротив, у самцов на 29-й день эксперимента вакцинация привела к изменению большинства биохимических параметров крови, АЛТ (F(2,12) = 7,65, p = 0,007], АСТ (F(2,12) = 8,13, p = 0,006), мочевина (F(2,12) = 6,5, p = 0,012] и уровень общего белка (F(2,12) = 5,2, p = 0,024]. Наши результаты показывают, что уровни мочевины, АЛТ и АСТ были повышены в обеих экспериментальных группах, вне зависимости от дозы мРНК-вакцины. В то же время на повышение и снижение уровня общего белка у экспериментальных групп выраженное влияние оказывала доза вводимой мРНК-вакцины.
Таким образом, иммунизация мРНК-вакциной MTB-mEp5-1 привела к выраженным зависимым от пола животных и дозы вакцины изменениям биохимических параметров крови в разных временных точках у самок и самцов крыс. В то же время влияние вакцинации MTB-mEp5-1 на гематологические параметры крови было умеренным (табл. 2).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Вакцинация зачастую приводит к побочным реакциям воспалительного генеза, которые могут включать боль в месте инъекции, покраснение или отек, а также системные симптомы, такие как повышение температуры тела и изменение клеточного состава крови [15]. мРНК-вакцины обладают иммуностимулирующими свойствами как за счет самой молекулы РНК, так и за счет компонентов липидных наночастиц [16]. Попадая в клетку, РНК может распознаваться внутриклеточными рецепторами, включая толл-подобные рецепторы 3 и 7, что приводит к активации сигнальных путей врожденного иммунитета [16, 17].
Мы показали, что через сутки после второго введения наибольшей дозы вакцинного препарата у самцов крыс наблюдается лимфоцитопения и нейтрофилия, которые нивелируются через две недели после введения мРНКвакцины. Эти данные хорошо согласуются с результатами доклинических исследований других мРНК-вакцинных препаратов, таких как RNA-1273, BNT162b2 [8, 9], в которых также в первые сутки после введения наблюдалось повышение уровня цитокинов в крови, увеличение количества лейкоцитов, нейтрофилов и эозинофилов, снижение лимфоцитов. Известно, что умеренный воспалительный ответ необходим для формирования адаптивного иммунитета. В недавнем исследовании [18] было также показано, что более выраженные воспалительные ответы на введение вакцины коррелируют с формированием более сильного адаптивного иммунного ответа. В нашем исследовании введение повышенной дозы (15 мкг) вакцины помимо изменения клеточного состава крови приводило к более выраженному адаптивному иммунному ответу.
В отличие от краткосрочных изменений гематологических параметров биохимические изменения, ассоциированные с воспалением, были более стабильными. По нашим данным, даже через 2 недели после второго введения препарата у самок был повышен уровень АЛТ, а у самцов были повышены АЛТ, АСТ, мочевина и снижен уровень общего белка. Изменения этих биохимических параметров могут быть связаны с нарушениями в работе печени и почек. Мы провели гистологический анализ органов животных (данные не представлены) и обнаружили микроскопические признаки воспаления в печени (дозозависимое нарастание признаков продуктивного васкулита: утолщение стенок сосудов, инфильтрация лимфоцитами, очаговые скопления лимфоцитов и макрофагов). В то же время в почках микроскопических признаков воспаления найдено не было.
Биохимические изменения в крови и микроскопические изменения печени были зарегистрированы также в доклинических исследованиях мРНК-вакцин, проведенных компаниями BioNTech и Moderna [8, 9]. В этих исследованиях у части животных также отмечались повышение уровня АСТ, мочевины, щелочной фосфатазы, триглицеридов, холестерина, билирубина и снижение уровня общего белка. Эти изменения сопровождались структурными изменениями в печени, которые заключались в увеличении массы органа, гепатоцитарной вакуолизации, гипертрофии клеток Купфера, единичных некрозах клеток или дегенерации гепатоцитов. Однако авторы не уточняют в доклиническом отчете, через какой период времени биохимические и гистологические показатели приходят в норму после вакцинации.
В доклиническом исследовании мРНК вакцины BNT162b2 авторы предполагают, что вакуолизация клеток печени может быть связана со специфическим накоплением ионизируемых липидов ALC-0315 [9]. Другие липидные компоненты, такие как SM102, ALC-0159 или PEG2000-DMG, также могут обладать токсичностью в больших дозах, однако используемые дозы в вакцине значительно меньше и предположительно не должны оказывать токсичных воздействий [8, 9, 19].
В нашей работе также были использованы липиды ALC-0315, SM-102, которые, как уже отмечалось, способны активировать врожденный иммунный ответ [16]. Значимым отличием нашей вакцины MTB-mEp5-1 от вакцин RNA-1273 и BNT162b2 является использование в последовательности РНК немодифицированного уридина. Последний является сильным стимулятором врожденного иммунитета в отличие от N1-метилпсевдоуридина, который был использован в вакцинах RNA-1273 и BNT162b2 [16, 17].
По всей вероятности, чрезмерная активация врожденного иммунитета как за счет немодифицированной РНК, так и за счет липидных компонентов может привести к более выраженному и продолжительному воспалительному процессу. Следует отметить, что чрезмерная иммунная активация может вызывать повреждение ткани печени и сопровождаться изменением биохимических параметров крови. Однако подобные случаи встречаются крайне редко (один на 14 млн случаев) при использовании различных вакцин, в том числе RNA-1273 и BNT162b2, и связаны с развитием аутоиммунных процессов [20].
Особого внимания заслуживают различия в выраженности влияния вакцинации MTB-mEp5-1 на биохимические параметры крови у самок и самцов. Наши результаты показывают, что через сутки после бустерной дозы мРНК вакцины различия в биохимических параметрах крови детектировались только у самок. В то же время через две недели после второй вакцинации более выраженные изменения детектировались у самцов. Эти различия могут быть обусловлены как различиями физиологических концентраций вакцины, связанными с весом животных (вес самцов был на 15–20% больше), так и другими физиологическими особенностями (уровень половых гормонов), генетическими различиями (включая экспрессию X-сцепленных генов) [21]. Различия в уровне половых стероидных гормонов оказывают влияние на функционирование иммунных клеток, что приводит к различиям в активности иммунного ответа [21]. В частности, результаты клинических исследований свидетельствуют о том, что у женщин наблюдается более высокий уровень выработки антител и более выраженный клеточный ответ после вакцинации [21, 22]. Вакцинация мРНК- или другими вакцинами приводит у женщин к более частым побочным эффектам, таким как повышение температуры тела, боль и местное воспаление [22, 23]. Таким образом, литературные данные о гендерспецифичных эффектах вакцинации согласуются с нашими результатами, которые показывают, что введение MTB-mEp5-1 вызывает у самок более быстрые изменения в биохимических параметрах крови. Эти изменения, по всей видимости, связаны с более высокой иммунореактивностью самок крыс на компоненты мРНК-вакцины.
ВЫВОДЫ
Результаты нашего исследования свидетельствуют о высокой реактогенности вакцины MTB-mEp5-1 на основе немодифицированной РНК. Признаки воспаления в исследованных органах и устойчивое изменение показателей биохимического анализа крови животных являются основанием для расширенного изучения безопасности и механизмов специфической фармакологической активности тестируемого препарата.
- Matarazzo L, Bettencourt PJG. mRNA vaccines: a new opportunity for malaria, tuberculosis and HIV. Front Immunol. 2023;14: 1172691.
- Kazakova A, Zhelnov P, Sidorov R, Rogova A, Vasileva O, et al. DNA and RNA vaccines against tuberculosis: a scoping review of human and animal studies Frontiers in Immunology. 2024; 15.
- Ndeupen S, Qin Z, Jacobsen S, Bouteau A, Estanbouli H, et al. The mRNA-LNP platform's lipid nanoparticle component used in preclinical vaccine studies is highly inflammatory. iScience. 2021; 24: 103479.
- Pateev I, Seregina K, Ivanov R, Reshetnikov V. Biodistribution of RNA Vaccines and of Their Products: Evidence from Human and Animal Studies. Biomedicines. 2023; 12.
- Kirshina AKA, Kolosova E, Imasheva E, Vasileva O, Zaborova O, Terenin I, Muslimov A, Reshetnikov V. Effects of various mRNALNP vaccine doses on neuroinflammation in BALB/c mice. RSMU. 2022; 6.
- van den Ouweland F, Charpentier N, Tureci O, Rizzi R, Mensa FJ, et al. Safety and reactogenicity of the BNT162b2 COVID-19 vaccine: Development, post-marketing surveillance, and real-world data. Hum Vaccin Immunother. 2024; 20: 2315659.
- Pang APS, Higgins-Chen AT, Comite F, Raica I, Arboleda C, et al. Longitudinal Study of DNA Methylation and Epigenetic Clocks Prior to and Following Test-Confirmed COVID-19 and mRNA Vaccination. Front Genet. 2022; 13: 819749.
- European Medicines Agency. Moderna Assessment Report COVID-19 Vaccine Moderna. 2021.
- European Medicines Agency. Assessment report: Comirnaty. 2021.
- Jin Z, Wu J, Wang Y, Huang T, Zhao K, et al. Safety and immunogenicity of the COVID-19 mRNA vaccine CS-2034: A randomized, double-blind, dose-exploration, placebo-controlled multicenter Phase I clinical trial in healthy Chinese adults. J Infect. 2023; 87: 556–70.
- Jackson LA, Anderson EJ, Rouphael NG, Roberts PC, Makhene M, et al. An mRNA Vaccine against SARS-CoV-2 - Preliminary Report. N Engl J Med. 2020; 383: 1920–31.
- Walsh EE, Frenck RW, Jr, Falsey AR, Kitchin N, Absalon J, et al. Safety and Immunogenicity of Two RNA-Based Covid-19 Vaccine Candidates. N Engl J Med. 2020; 383: 2439–50.
- Reshetnikov V, Terenin I, Shepelkova G, Yeremeev V, Kolmykov S, et al. Untranslated Region Sequences and the Efficacy of mRNA Vaccines against Tuberculosis. Int J Mol Sci. 2024; 25.
- Vasileva O, Krapivin B, Muslimov A, Kukushkin I, Pateev I, Rybtsov S, et al. Immunogenicity of full-length and multi-epitope mRNA vaccines for M. Tuberculosis as demonstrated by the intensity of T-cell response: a comparative study in mice. Bulletin of RSMU. 2023; 03: 42–48.
- Teijaro JR, Farber DL. COVID-19 vaccines: modes of immune activation and future challenges. Nat Rev Immunol. 2021; 21: 195–7.
- Verbeke R, Hogan MJ, Lore K, Pardi N. Innate immune mechanisms of mRNA vaccines. Immunity. 2022; 55: 1993–2005.
- Muslimov A, Tereshchenko V, Shevyrev D, Rogova A, Lepik K, et al. The Dual Role of the Innate Immune System in the Effectiveness of mRNA Therapeutics. Int J Mol Sci. 2023; 24.
- Zhuang CL, Lin ZJ, Bi ZF, Qiu LX, Hu FF, et al. Inflammationrelated adverse reactions following vaccination potentially indicate a stronger immune response. Emerg Microbes Infect. 2021; 10: 365–75.
- Kang DD, Hou X, Wang L, Xue Y, Li H, et al. Engineering LNPs with polysarcosine lipids for mRNA delivery. Bioact Mater. 2024; 37: 86–93.
- Schinas G, Polyzou E, Dimakopoulou V, Tsoupra S, Gogos C, et al. Immune-mediated liver injury following COVID-19 vaccination. World J Virol. 2023; 12: 100–8.
- Flanagan KL, Fink AL, Plebanski M, Klein SL. Sex and Gender Differences in the Outcomes of Vaccination over the Life Course. Annu Rev Cell Dev Biol. 2017; 33: 577–99.
- Klein SL, Jedlicka A, Pekosz A. The Xs and Y of immune responses to viral vaccines. Lancet Infect Dis. 2010; 10: 338–49.
- Bignucolo A, Scarabel L, Mezzalira S, Polesel J, Cecchin E, et al. Sex Disparities in Efficacy in COVID-19 Vaccines: A Systematic Review and Meta-Analysis. Vaccines (Basel). 2021; 9.