Статья размещена в открытом доступе и распространяется на условиях лицензии Creative Commons Attribution (CC BY).
ОРИГИНАЛЬНОЕ ИССЛЕДОВАНИЕ
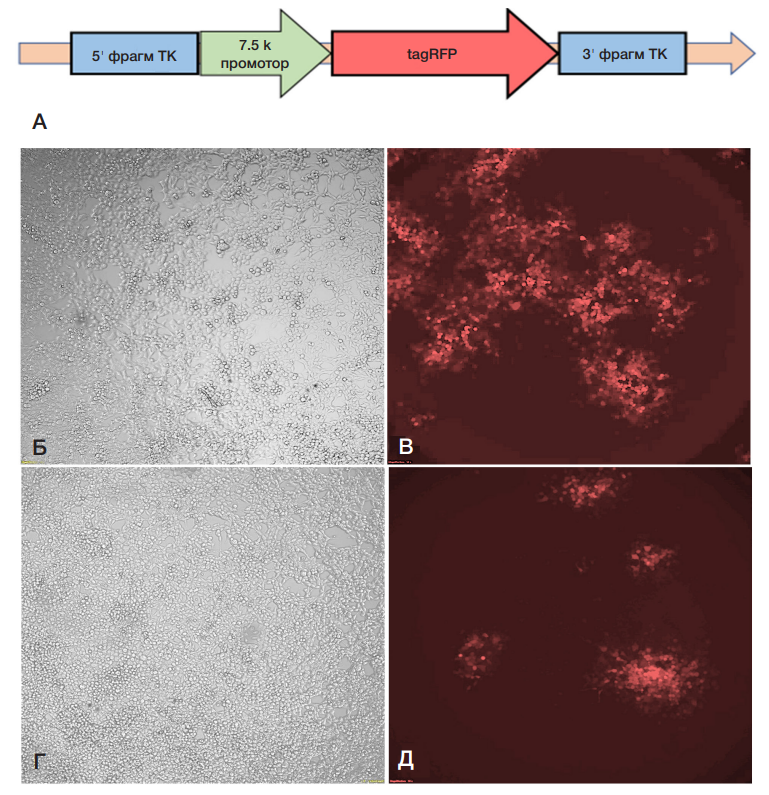
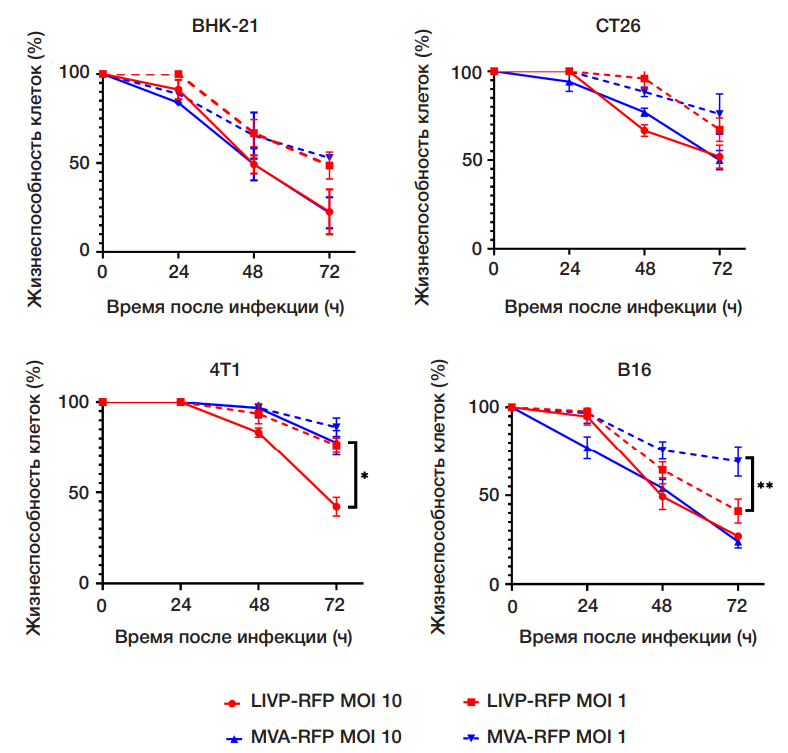
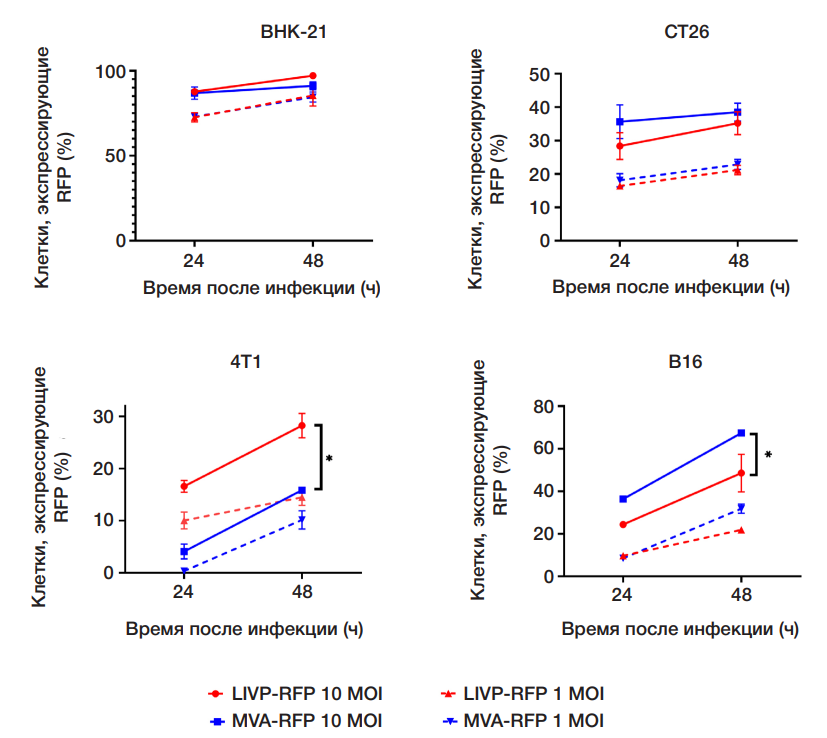
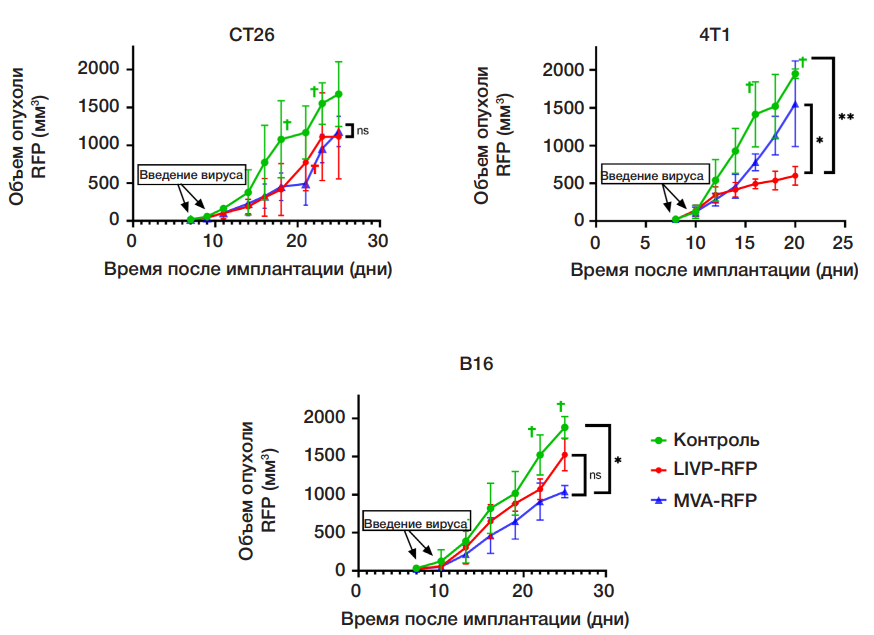
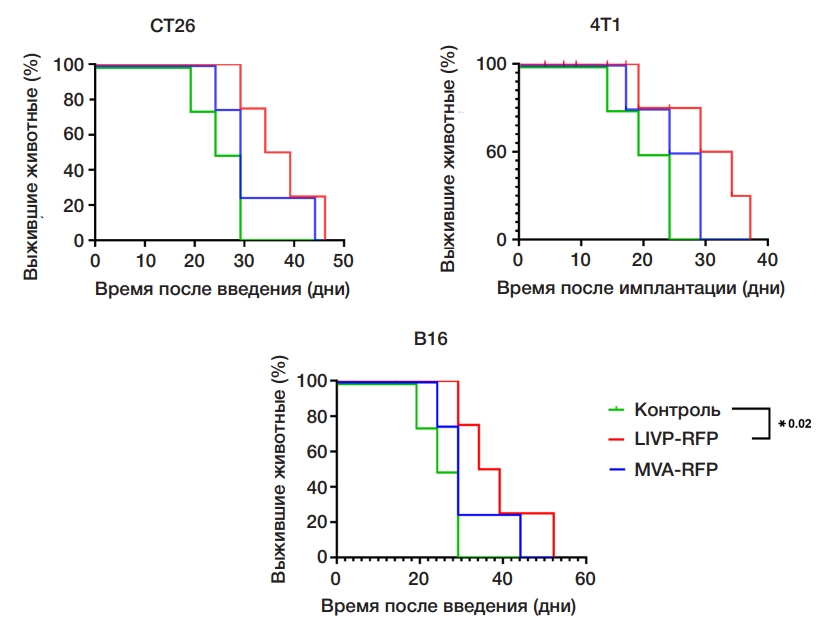
Сравнение онколитической активности рекомбинантных штаммов вируса осповакцины LIVP-RFP и MVA-RFP в отношении солидных опухолей
1 Институт молекулярной биологии имени Энгельгардта, Российской академии наук, Москва, Россия
2 Московский физико-технический институт, Долгопрудный, Россия
3 Федеральный научно-клинический центр специализированных видов медицинской помощи и медицинских технологий Федерального медико-биологического агентства, Москва, Россия
Для корреспонденции: Анастасия Валерьевна Липатова
ул. Вавилова, д. 32, г. Москва, 119991, Россия; moc.liamg@vnaavotapil
Финансирование: разработка онколитических вирусов и эксперименты in vitro были выполнены при поддержке Российского научного фонда (грант РНФ № 20-75-10157); эксперименты in vivo также выполнены при поддержке Российского научного фонда (грант РНФ № 22-64-00057).
Вклад авторов: Я. Шакиба — анализ литературы, выполнение преаналитического этапа работы, проведение экспериментов in vitro и in vivo, анализ и интерпретация данных, подготовка рисунков и графиков; Е. Р. Набережная — проведение экспериментов in vitro, анализ и интерпретация данных; Д. В. Кочетков — уход за животными, интерпретация данных, Г. М. Юсубалева — визуализация данных, редактирование рукописи; П. О. Воробьев — наработка препаративных количеств вируса для in vivo исследований; В. П. Баклаушев — планирование исследования, выполнение преаналитического этапа работы, анализ данных; А. В. Липатова — руководство исследованием, разработка дизайна, создание рекомбинантных штаммов, интерпретация данных, редактирование рукописи.
Соблюдение этических стандартов: исследование одобрено этическим комитетом ИМБ РАН (протокол № 3 от 27 октября 2022 г.). Эксперименты проводили в соответствии с директивой Европейского парламента и Совета Европейского союза 2010/63/ЕС о защите животных, используемых для исследований.